|
|
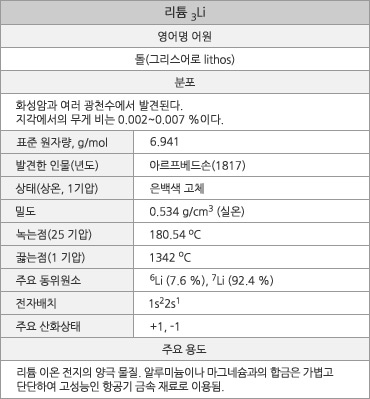
원자번호 3번, 리튬. |
리튬 원소 정보. |
리튬의 발견

|
|
|
|
리튬의 불꽃 반응. 진한 붉은색을 띤다. |
기름에 떠 있는 리튬의 모습. 리튬은 금속 원소 중에서 가장 가볍다. <출처: (CC)W.Oelen at Wikipedia.org> |
|

2Li + RX → RLi + LiX (R은 알킬, X는 할로겐 원소)

|
리튬의 생산

|
|

6Li + 1n → 4He + 3H
2H + 3H → 1n + 4He

|
|
6Li의 중수소화물은 수소폭탄의 연료로 사용되었다. |
리튬은 의학용으로 항 우울제로 사용된다. |
|
|
주로 휴대용 전자 제품에서 사용되고 있는 리튬 이온 2차 전지. <출처: (CC)Kristoferb at Wikipedia.org> |
현재 확인된 리튬의 매장량은 전기 자동차 약 40억 대의 전지로 사용되기에 충분한 양이다. <출처: (CC) frankh at Wikipedia.org> |
|
- 수치로 보는 리튬
리튬의 표준원자량은 6.941g/mol이며, 녹는점은 180.54oC이고 끓는점은 1342oC이다. 전자배열은 1s22s1이며, 이온화 에너지는 530.2kJ/mol(소듐은 495.8kJ/mol)이다. 밀도는 실온에서 0.534g/cm3으로 물의 약 1/2이며 금속 중에서 가장 가볍고, 고체 원소 중에서 가장 낮다. 비열은 실온에서 3.58J·g-1·K-1(0.856cal·g-1·K-1)로 금속 중에서 가장 크다. 리튬 불꽃의 파장은 670.8nm이다. LI+ 이온의 반경은 76pm(1pm=1x10-12m)로 Mg2+ 이온의 반경(72pm)과 비슷하다. 추정 회수 가능 매장량은 약 3,500만 톤이며 이중 70% 이상이 칠레, 볼리비아, 아르헨티나에 있다. 바닷물에는 0.1~0.2ppm(물 1L당 0.1~0.2mg)이 녹아 있다.
- 알칼리 금속
1족 원소로 리튬(Li), 소듐(Na), 포타슘(K), 루비듐(Rb), 세슘(Cs), 프랑슘(Fr)이 이에 속한다. 전자배치는 각 원소보다 원자 번호가 하나 적은 비활성 기체의 전자배치에 추가로 1개의 전자가 다음 전자껍질의 s 오비탈에 있다. 따라서 알칼리 금속들은 쉽게 1개의 전자를 잃고 +1가 이온이 된다. 좋은 전기 및 열 전도체이고 화학 반응성이 크다.
발행일 2011.09.01
Lithium
| Atomic Weight | 6.941 | |
| Density | 0.535 g/cm3 | |
| Melting Point | 180.54 °C | |
| Boiling Point | 1342 °C | |
| Full technical data | ||
The lightest metal, lithium easily floats on water, which it reacts with, skittering around releasing hydrogen gas. It's soft enough to cut with hand shears, leaving marks such as you see on this sample.
Scroll down to see examples of Lithium.
'Natural science > 화 학' 카테고리의 다른 글
| Boron ( B ), 5 - 붕소 (0) | 2012.03.01 |
|---|---|
| Beryllium ( Be ), 4 - 베릴륨 (0) | 2012.03.01 |
| 삼중수소 (0) | 2012.03.01 |
| 원소의 기원 (0) | 2012.03.01 |
| Helium ( He ), 2- 헬륨 (0) | 2012.03.01 |