|
|
원자번호 6번, 탄소. 다이아몬드는 탄소의 대표적인 동소체다. <출처: gettyimages> |
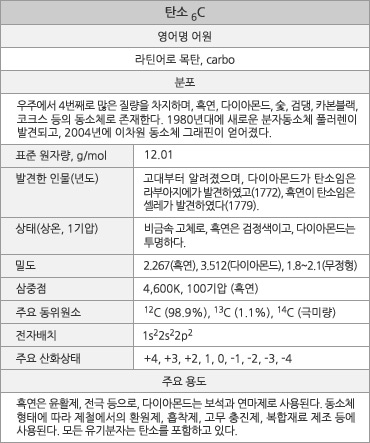
탄소의 원소 정보. |
|
|
라부아지에. 다이아몬드와 숯이 화학적으로는 같은 원소임을 밝혔다. |
셸레. 흑연이 탄소의 또 다른 형태임을 확인하였다. |
|
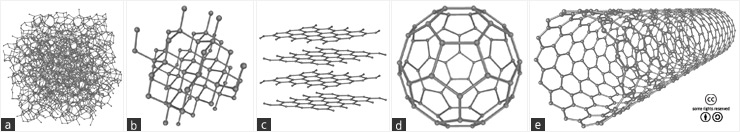
(a) 무정형 탄소 (b) 다이아몬드 (c) 흑연 (d) C60 (e) 탄소 나노튜브. <출처: (CC)mstroeck at Wikipedia.org>
|
|
탄소는 석탄, 석유, 천연가스와 같은 화석연료의 주된 구성 원소이다. <출처: gettyimages> |
탄소의 동소체 흑연은 연필심, 브레이크 라이닝, 내화물, 윤활제 등으로 사용된다. <출처: gettyimages> |
|
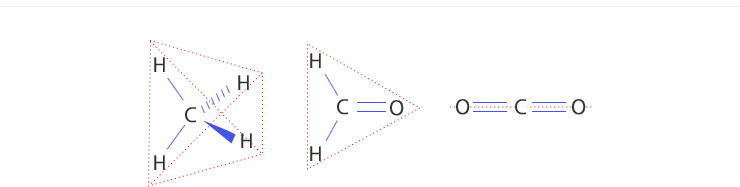
탄소 원자에 결합된 원자의 수와 구조의 관계를 보이는 예.

|


|
|
코크스는 철광석으로부터 산소를 떼어내고 용광로의 온도를 높게 유지하는데 이용된다. |
합성 다이아몬드 날로 만들어 진 메스. 다이아몬드는 단단한 성질을 이용한 각종 절삭 공구와 연마제로 사용된다. |
|
- 수치로 보는 탄소
탄소의 표준원자량은 12.0107g/mol이다. 물리적 성질은 동소체에 따르다. 전자배열은 1s22s22p2이다. 1기압에서는 녹지 않으며, 삼중점은 흑연의 경우 100기압, 4,600K이고, 승화 온도는 약 3,900K이다. 실온에서의 밀도는 무정형 탄소는 1.8~2.1g/cm3, 흑연은 2.267g/cm3, 그리고 다이아몬드는 3.514g/cm3이다. 자연상태에서 3가지 동위원소가 존재하는데, 이들은 12C(98.93%), 13C(1.07%), 14C(약 1x10-10%)이다. 12C 원자의 질량은 원자질량단위의 기준이 되며, 14C는 반감기가 5,760년인 방사성 동위원소로 탄소 연대 측정에 이용된다. 제1, 2, 3, 4 이온화 에너지는 각각 1,086.5, 2,352.6, 4,620.5, 6,222.7kJ/mol이다. 전기 비저항은 흑연은 (0.4~5.0)x10-4ohm∙cm(평면 층에서)이고, 다이아몬드는 1014~1015 ohm∙cm이다. 27oC에서의 열전도도는 흑연이 119~165W∙m-1∙K-1, 다이아몬드는 900~2,300W∙m-1∙K-1이다.
- 동소체(allotrope)
같은 화학 원소이면서 구조와 성질이 다른 것들을 동소체라 한다. 흑연, 다이아몬드, 숯, 검댕이 자연 상태에서 존재하는 탄소 동소체이며, 풀러렌, 그래핀이 인공적으로 만든 탄소 동소체이다.
발행일 2011.09.28
Carbon
| Atomic Weight | 12.0107 | |
| Density | 2.26 g/cm3[note] | |
| Melting Point | 3550 °C[note] | |
| Boiling Point | 4027 °C[note] | |
| Full technical data | ||
A diamond is forever, unless you heat it too much and it burns up into carbon dioxide gas. Graphite is also pure carbon and widely used in pencils, but not nearly as pretty. In this poster, pretty trumps practical.
Scroll down to see examples of Carbon
'Natural science > 화 학' 카테고리의 다른 글
| 질소의 순환 (0) | 2012.03.01 |
|---|---|
| Nitrogen ( N ), 7 - 질소 (0) | 2012.03.01 |
| Boron ( B ), 5 - 붕소 (0) | 2012.03.01 |
| Beryllium ( Be ), 4 - 베릴륨 (0) | 2012.03.01 |
| Lithium ( Li ), 3 - 리튬 (0) | 2012.03.01 |