|
|
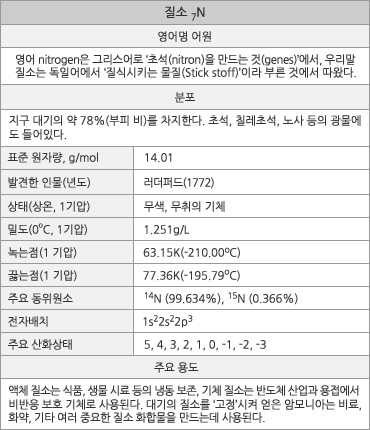
원자번호 7번, 질소. |
질소의 원소 정보. |
|
|
질소를 발견한 스코틀랜드의 대니얼 러더퍼드. |
암모니아 합성법을 개발한 독일의 프리츠 하버. |
|
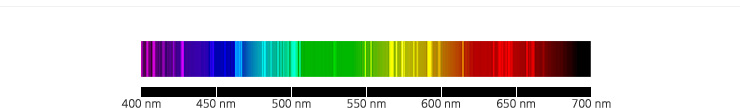
질소의 선 스펙트럼.

|
|
액체 질소는 끓는점이 낮고 반응성이 거의 없기 때문에 시료를 조직이 파괴되지 않는 상태로 급속 동결한다. |
나이트로 화합물은 폭약으로 사용된다. 트라이나이트로톨루엔(TNT)의 폭발 모습. |
|
|
질소 비료의 사용으로 인류에게 풍부한 먹거리를 제공하는 녹색혁명이 가능케 되었다. |
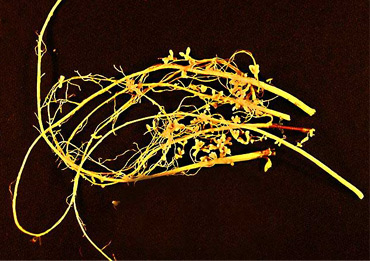
콩의 뿌리혹에 공생하는 질소고정 박테리아. |
|
- 수치로 보는 질소
질소의 표준원자량은 14.0067g/mol이다. 전자배열은 1s22s22p3이다. 원소 상태는 이원자 분자인 N2이며, 이는 건조된 공기 부피의 78.08%(무게 비로는 75.3%)를 차지한다. N2에서 질소-질소 결합은 삼중 결합이고, 이의 해리에너지는 945.41kJ/mol로 매우 강한 결합이다. 1기압에서 녹는점은 63.15K(-210.00oC)이고 끓는점은 77.36K(-195.79oC)이다. 0oC, 1기압에서 기체 밀도는 1.251g/L이며, 끓는점에서의 액체 밀도는 0.808g/cm3이다. 자연상태에서 14N(99.634%)와 15N(0.366%)의 두 가지 동위원소가 존재한다. 제1, 2, 3 이온화 에너지는 각각 1402.3, 2856, 4578.1kJ/mol이다.
- 전기음성도 (Electronegativity)
분자에서 어떤 원자가 자신에게로 전자를 끌어들이는 경향을 수치화 한 것으로, 1932년에 폴링이 제안하였다. 플루오르(F)가 4.0으로 가장 크고, 프랑슘(Fr)이 0.70으로 가장 작다. 주기율표에서 같은 족에 속하는 원소들은 원자번호가 클수록 작은 값을 가지며, 같은 주기의 원소들은 족의 번호가 클수록 큰 값을 갖는다 (전이금속들 사이에서는 순서가 바뀌는 경우가 있다).
발행일 2011.10.05
Nitrogen
| Atomic Weight | 14.0067 | |
| Density | 1.251 g/l[note] | |
| Melting Point | -210.1 °C | |
| Boiling Point | -195.79 °C | |
| Full technical data | ||
Colorless nitrogen gas makes up 78% of the atmosphere, but here we see it in liquid form at -196DegreeC. It is boiling off, creating a visible vapor--not of steam, but of water condensed from the surrounding air.
Scroll down to see examples of Nitrogen.
'Natural science > 화 학' 카테고리의 다른 글
| Oxygen ( O ), 8 - 산소 (0) | 2012.03.01 |
|---|---|
| 질소의 순환 (0) | 2012.03.01 |
| Carbon ( C ), 6 - 탄소 (0) | 2012.03.01 |
| Boron ( B ), 5 - 붕소 (0) | 2012.03.01 |
| Beryllium ( Be ), 4 - 베릴륨 (0) | 2012.03.01 |