|
|
원자번호 12번, 마그네슘. 마그네슘은 가볍고 단단하기 때문에 자동차나 항공기 부품 등에 사용된다. 사진은 마그네슘 합금 바디로 만들어진 경주용 자동차, 메르세데스 벤츠 300 SLR. <출처: (CC)LSDSL at Wikipedia.org> |
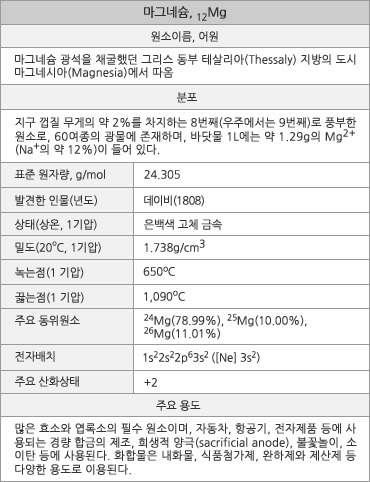
마그네슘의 원소 정보. |
|
|
조셉 블랙은 1755년 마그네슘이 원소라는 사실을 밝혔다. |
험프리 데이비는 1808년 금속 마그네슘을 최초로 분리하였다. |
|
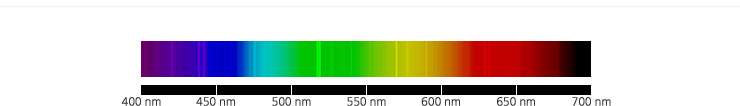
마그네슘의 선 스펙트럼.

마그네슘의 화학 반응성

|
|
|
|
마그네슘은 쉽게 불이 붙는 성질을 가지고 있어, 점화기(fire starter)로 사용된다. <출처: (CC)Hiroaki Nakamura at Wikipedia.org> |
공기 중에서 발화하면 자외선을 포함하는 밝은 흰빛이 나오는 마그네슘의 성질은 불꽃놀이에 이용된다. |
|
|
|
|
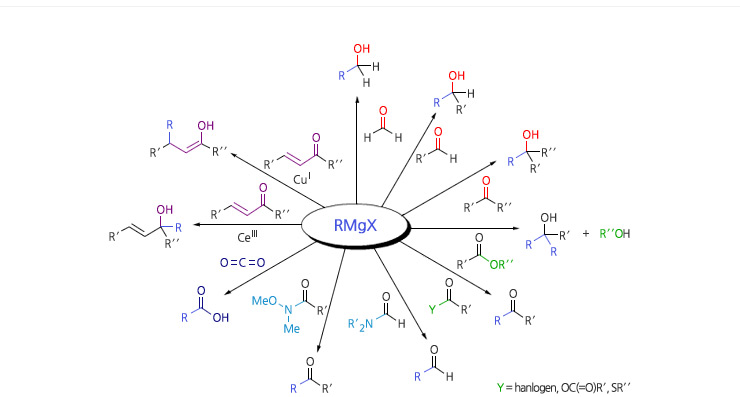
카르보닐 화합물의 그리냐르 반응의 예. 그리냐르 시약은 다른 여러 범주의 화합물과도 반응하여 이들을 다른 화합물로 변환시킨다.

|
|
|
|
|
식물에서 마그네슘이 결핍되면 잎이 누렇게 되고 심하면 식물 조직이 죽게 된다. |
마그네슘은 양념, 견과류, 곡물, 차, 채소 등에 많이 들어 있다. |
|
- 수치로 보는 마그네슘
마그네슘의 표준원자량은 24.305g/mol이다. 원자의 전자배치는 1s22s22p63s2 ([Ne]3s2)이며, 화합물에서의 주된 산화수는 +2다. 지각에 약 2% 무게비로 존재하며 8번째로 풍부한 원소이다. 인체에서는 11번째로 풍부한 원소이다. 바닷물 1L에는 약 1.29g이 들어있다. 1기압에서 녹는점은 650oC(참고로 알루미늄의 녹는점은 660oC)이고 끓는점은 1,090oC이다. 실온에서 밀도는 1.738g/cm3로, 알루미늄의 2/3, 타이타늄의 1/3, 그리고 철의 1/4이다. MgO로의 연소열은 24.76J/g(5.9cal/g)이고, 녹음열과 증발열은 각각 8.48kJ/mol과 128kJ/mol로, 2족 원소 중에서 녹음열은 Be 다음으로 크나 증발열은 가장 작다. 자연 상태에서는 24Mg, 25Mg, 26Mg가 대략 8:1:1로 존재한다. 첫 번째와 두 번째 이온화 에너지는 737.7kJ/mol과 1,450.7kJ/mol이다.
Magnesium
| Atomic Weight | 24.305 | |
| Density | 1.738 g/cm3 | |
| Melting Point | 650 °C | |
| Boiling Point | 1090 °C | |
| Full technical data | ||
These magnesium nodules grow during the refining process. Usually they are melted down into useful products such as lightweight race car components and fire starters. Thin strips light easily and burn brightly.
Scroll down to see examples of Magnesium.