|
|
원자번호 26번, 철. <출처: (CC)Cezary p at wikipedia.org> |
철의 원소 정보. |
|
철의 역사

|
|
|
|
초기의 철 야금은 내화성이 있는 흙이나 돌로 만든 연로에서 목탄을 태워 철광석을 철로 환원시키는 것이었다. 사진은 중세 유럽의 연로 제련 모습. |
현대 제철의 주된 방법이 되는 고로법은 용광로를 사용한 것으로, 초기에는 용광로의 연료로 목탄을 사용하다가, 석탄을 거쳐 코크스를 사용하게 된다. 사진은 중국의 명 왕조 때 제철에 용광로를 이용하는 모습. |
|
|
1855년, 영국인 베세머가 불순물을 쉽게 제거할 수 있는 베세머 전로를 발명하여 철강 생산은 아주 값싸고 간단한 조작으로 가능하게 되었다. |
부식성을 해결한 스테인레스강(stainless steel)은 1913년에 처음으로 만들어져 1930년대 이후에 본격적으로 사용되게 되었다. <출처: sxc.hu> |
|
철의 화학적 특성

|
|
|
|
|
|
|

프러시안 블루.
|
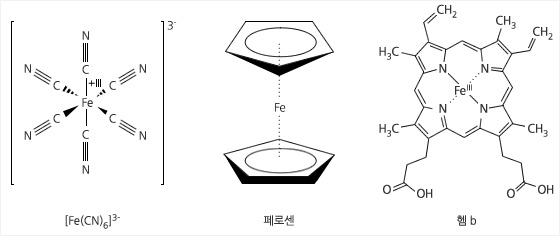
철 배위화합물의 몇 가지 예.
|
강자성체와 액체 자석

|
|
|
|
|
현대적 제철소. |
선철은 4~5%의 탄소를 포함하고 있어 단단하나 잘 부서진다. <출처: (CC)Mfields1 at Wikipedia.org> |
|


철은 전세계 금속 생산량의 약 95%을 차지할 정도로 많이 생산되어 사용된다. <출처: gettyimages>
|
- 수치로 보는 철
철의 표준원자량은 55.845g/mol이다. 원자의 바닥 상태 전자배치는 1s22s22p63s23p63d64s2 ([Ar]3d64s2)이다. 우주에서는 6번째로 풍부하고, 지구 전체 무게의 약 35%를 차지하며, 지각에서의 무게비는 약 5%로 산소(47%), 규소(28%), 알루미늄(8.4%) 다음으로 풍부한 원소이다. 흙에는 0.5~5%, 바닷물에는 대략 2.5 ppb(1 ppb는 10억 분의 1) 농도로 들어있다. 녹는점은 1538oC이고 끓는점은 2862oC이며, 20oC에서 밀도는 7.874g/cm3이다. 20oC에서 전기 비저항은 96.1nΩ∙m이다. 첫 번째, 두 번째, 세 번째 이온화 에너지는 각각 762.5, 1561.9, 2957kJ/mol이고, 폴링의 전기음성도는 1.83이다. 천연 상태의 동위원소는 54Fe(5.8%), 56Fe(91.72%), 57Fe(2.2%), 58Fe(0.28%)이다.
- 전이금속원소
원자의 d 부껍질에 전자가 부분적으로 채워져 있거나, d 부껍질이 부분적으로 채워진 양이온을 만드는 원소. 첫 번째 계열은 3d 부껍질에 전자가 부분적으로 채워진 것으로, 원자번호 21번의 스칸듐(Sc)에서 원자번호 30번의 아연(Zn)까지의 원소이다.
- 강자성(Ferromagnetic)과 퀴리 온도
강자성은 외부에서 자기장을 걸어주면 그 자기장의 방향으로 자기화된 뒤, 외부 자기장을 제거하여도 자기화가 남아 있는 성질이다. 강자성 물질은 영구자석이 될 수 있다. 어떤 물질이 강자성을 띨 수 있는 가장 높은 온도를 그 물질의 퀴리 온도라 한다. 철의 퀴리 온도는 770oC이다.
- 화합물에서 원소의 산화 수 나타내기
화합물에서 어떤 원소의 산화 수를 나타내는 보편적 방법은 원소명 다음의 괄호 속에 로마 숫자로 산화 수를 적는 것이다. 다른 방법은, 철처럼 한 원소에서 2가지의 흔한 산화 상태가 있을 때, 낮은 산화 상태에 ‘제1’을, 높은 것에 ‘제2’를 원소 이름 앞에 붙이고, 영어식 이름에는 접미어로 ‘ous’와 ‘ic’을 각각 사용한다. 예로 FeCl2은 염화철(II) 또는 염화제1철로, 그리고 FeCl3는 염화철(III) 또는 염화제2철로 부른다. 영어식 이름은 각각 ferrous chloride와 ferric chloride이다.
- 배위화합물
금속 원자나 이온이 전자 쌍을 제공하는 몇 개의 음이온 또는 중성분자(이들을 배위자라 한다)와 배위공유결합(결합에서 공유하는 전자쌍을 모두 배위자에서 제공하여 만든 결합)을 하고 있는 화합물.
발행일 2011.12.28
Iron
| Atomic Weight | 55.845 | |
| Density | 7.874 g/cm3 | |
| Melting Point | 1538 °C | |
| Boiling Point | 2861 °C | |
| Full technical data | ||
This meteorite, part of one that fell in Xiquipilco, Mexico in ancient times, is made mostly of iron. Locals created iron tools from it for generations before the first samples made their way out in the 1700s.
Notes on the properties of Iron:
Specific Heat: Value given for solid phase.
Up to date, curated data provided by Mathematica's ElementData function from Wolfram Research, Inc.
'Natural science > 화 학' 카테고리의 다른 글
| Oxidation (산화반응) (0) | 2012.03.01 |
|---|---|
| reduction (환원반응) (0) | 2012.03.01 |
| Manganese ( Mn ), 25- 망간, 망가니즈 (0) | 2012.03.01 |
| 계면활성제 (0) | 2012.03.01 |
| Chromium ( Cr ), 24- 크롬 (0) | 2012.03.01 |







 [Fe(CN)6]3-
[Fe(CN)6]3- 



