|
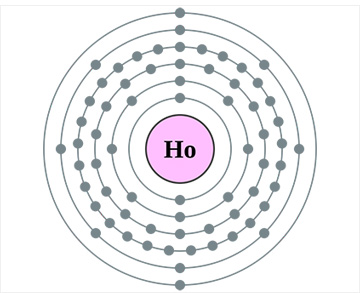
홀뮴은 비교적 무른 은백색 금속으로 연성과 전성이 있다. 녹는점은 1470oC이고, 끓는점은 2700oC이며, 25oC에서 밀도는 8.795g/cm3이다. 133K 이상에서는 상자성(paramagnetic)이며, 20~133K에서는 반강자성(antiferromagnetic)이고, 20K이하에서는 강자성(ferromagnetic)이다. 천연 원소 중에서는 자기 모멘트(magnetic moment)2)가 가장 크다. 결정은 육방조밀격자(hcp) 구조를 한다. 홀뮴은 실온의 건조한 공기 중에서는 비교적 안정하나, 습기가 있거나 가열하면 쉽게 산화되어 노란색의 산화홀뮴(Ho2O3)이 된다. 화합물에서의 산화수는 주로 +3이며, 대부분의 홀뮴 화합물들은 갈색을 띠는 노랑색이다. 물과 반응하여 수소 기체를 발생시키고 수산화홀뮴(Ho(OH)3)이 된다. 산과 반응하여 수소를 발생시키면서 녹으며, 다른 배위자가 없으면 Ho3+ 이온은 수용액에서 노란색의 [Ho(H2O)9]3+으로 존재한다.
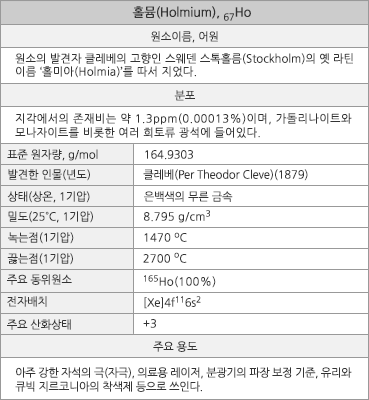
홀뮴의 지각에서의 존재비는 약 1.3ppm(0.00013%)이다. 홀뮴은 오도-하킨스 규칙(Oddo-Harkins rule)3)에 따라 원자번호가 짝수인 이웃 원소 디스프로슘(Dy)과 어븀(Er)보다는 존재량이 적으나, 원자번호가 홀수인 중란타넘족 원소(65Tb, 67Ho, 69Tm, 71Lu) 중에서는 존재량이 가장 많은데, 이는 수은(Hg), 금(Au), 은(Ag), 안티모니(Sb), 비스뮤트(Bi), 아이오딘(I)보다 많은 양이다. 홀뮴은 이트륨(Y) 함량이 높은 희토류 광석인 제노타임(xenotime), 가돌리나이트(gadolinite), 육세나이트(euxenite), 퍼거소나이트(fergusonite) 등에 대략 1%까지 들어있다. 대표적인 희토류 광석인 모나자이트(monazite)와 희토류광((bastnäsite)에는 단지 0.001%~0.1%의 비율로 들어 있으나, 이들 광석에서 다른 희토류 원소들을 생산할 때 홀뮴을 부산물로 얻는다. 최근에는 중국 남부의 이온-흡착 점토들도 희토류의 주요 자원이 되었는데, 이들은 제노타임이나 가돌리나이트와 비슷한 희토류 원소 조성을 갖고 있다. 원래의 점토에는 희토류가 0.1% 정도 들어있으나, 쉽게 농축될 수 있으며 전체 희토류의 약 65%를 이트륨이 차지하고 홀뮴은 약 1.5%를 차지한다. 홀뮴의 전세계 년간 생산량은 약 10톤이고, 광석 매장량은 40만 톤으로 추정되는데, 수요가 많거나 공급이 부족한 희토류 원소는 아니다.
홀뮴은 자기의 세기가 가장 커질 수 있는 원소로, 아주 강한 전자석의 자극 또는 자속 유도기(magnetic flux concentrator)로 사용된다. 그리고 여러 고체상태 레이저에 사용되는데, 홀뮴 레이저는 암세포의 사멸, 신장 결석의 파괴, 비대해진 전립선 및 치과 처치 등 여러 의료용 목적으로 널리 사용된다. 홀뮴 염 용액과 홀뮴 유리는 분광기의 자외선/가시광선 영역의 파장 보정에서 기준 물질로 사용된다. 홀뮴은 또한 인조 보석인 큐빅 지르코니아의 채색재의 하나로 사용되며, 중성자를 잘 흡수하므로 원자로 제어봉에 사용되기도 한다. |


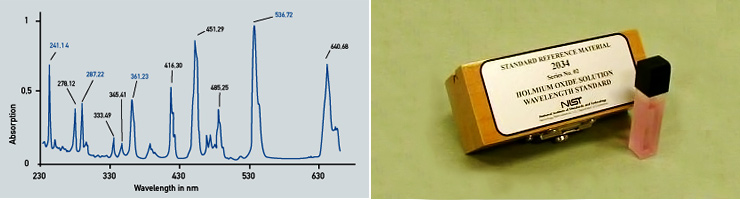

 수치로 보는 홀뮴
수치로 보는 홀뮴
 자기 모멘트(magnetic moment)와 보어 마그네톤(Bohr magneton)
자기 모멘트(magnetic moment)와 보어 마그네톤(Bohr magneton)
 오도-하킨스 규칙(Oddo-Harkins rule)
오도-하킨스 규칙(Oddo-Harkins rule)



 Ho Eo
Ho Eo