|
|
|
원자번호 66번, 디스프로슘 <출처 : 닛산> |
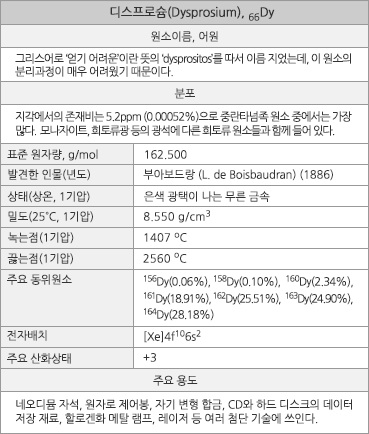
디스프로슘의 원소 정보 |
|

풍력 발전. 풍력 발전기에 사용되는 네오디뮴 자석에서는 네오디뮴의 약 4-5%가 디스프로슘으로 치환되어 있다. <출처: (cc) Kim Hansen>
|
|
|
|

디스프로슘은 밝은 은색 광택이 나는 금속으로, 칼로 자를 수 있을 정도로 무르다. <출처: (cc) Materialscientist at en.wikipedia>
|
|
|
|
|
|

모자나이트 광석. 디스프로슘은 주로 모나자이트와 희토류광에서 분리·생산된다 <출처: (cc) Rob Lavinsky / iRocks.com>
|

하이브리드 자동차의 엔진-모터 시스템. 하이브리드 자동차의 드라이버 모터 자석에는 1대 당 약 100g의 디스프로슘이 들어가는데, 하이브리드 자동차의 생산 확대로 가까운 장래에 디스프로슘의 공급 부족이 예상된다.
|

하드 디스크. 디스프로슘은 자화율이 커서 하드디스크 등의 데이터 저장 매체로 사용된다. (google-dysprosium- image)
|

황산디스프로슘(Dy2(SO4)3) <출처: (cc) images-of-elements.com>
|
 수치로 보는 디스프로슘
수치로 보는 디스프로슘
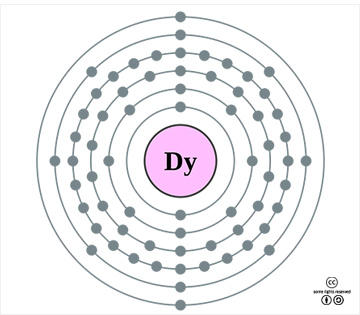
디스프로슘의 표준원자량은 162.500g/mol이고, 원자의 바닥 상태 전자배치는 1s22s22p63s23p63d104s24p64d105s25p64f106s2 ([Xe]4f106s2)이며, 화합물에서 주된 산화 수는 +3이다. 지각에서의 존재 비는 약 5.2ppm(0.00052%)이다. 3가지 동소체가 있으며, 결정은 실온에서 육방조밀격자(hcp) 구조를 한다. 1기압에서 녹는점은 1407oC이고 끓는점은 2560oC이며, 25oC에서의 밀도는 8.550g/cm3이고 녹는점에서의 액체 밀도는 8.37g/cm3이다. 85K 이하에서는 강자성을, 85~179K에서는 반강자성을, 그리고 179K 이상에서는 상자성을 보인다. 첫 번째, 두 번째, 세 번째 이온화 에너지는 각각 573.0, 1130, 2200kJ/mol이며, 폴링의 전기 음성도는 대략 1.22이다. 원자 반경은 178.1pm(비교: Tb, 177.3pm; Ho, 176.2pm)이며, 6배위체의 Dy3+ 이온 반경은 91.2pm(비교: Tb3+, 92.3pm; Ho3+, 90.1pm)이다. Dy4+/Dy3+의 표준환원 전위는 5.4V로 추정되고, Dy3+/Dy2+와 Dy3+/Dy의 표준 환원 전위는 각각 -2.5V와 -2.29V이다. 천연상태 동위원소는 156Dy(0.06%), 158Dy(0.10%), 160Dy(2.34%), 161Dy(18.91%), 162Dy(25.51%), 163Dy(24.90%), 164Dy(28.18%)의 7가지이다. 가격은 2003년~2011년 기간에 약 130배가 뛰었다.
 자화율(magnetic susceptibility)
자화율(magnetic susceptibility)
물질이 외부에서 걸어준 자기장에 의해 자기화(자화)되는 정도를 나타내는 것으로, 자기장(H)에 대한 자기화(M)의 비율(M/H)로 정의된다. 부호는 상자성(paramagnetic) 물질은 양(+)이고, 반자성(diamagnetic) 물질은 음(-)이다.
 보자력(coercivity)
보자력(coercivity)
강자성체(자석 물질)를 자기유도가 포화된 상태에서 자화 정도를 0으로 내리기 위해 자화 방향과 반대로 걸어주어야 하는 소거 자기장의 세기로, 자석 물질이 자기소거에 저항하는 척도이다. 항자기력이라고도 한다.
발행일 2012.12.19
Dysprosium
Dysprosium compounds are used in the coatings of many hard disk drives to record digital data as field orientations in nanoscale magnetic domains. Other than that, dysprosium has few applications. Scroll down to see examples of Dysprosium | |||||||||||||||||
'Natural science > 화 학' 카테고리의 다른 글
| MSG (0) | 2012.12.28 |
|---|---|
| Holmium(Ho), 67-홀뮴 (0) | 2012.12.28 |
| Terbium(Tb), 65-터븀(테르븀) (0) | 2012.12.28 |
| Gadolinium(Gd), 64-가돌리늄 (0) | 2012.12.26 |
| Europium(Eu), 63-유로퓸 (0) | 2012.12.26 |




 Dy3+ Eo = 5.4 V(추정)
Dy3+ Eo = 5.4 V(추정)