|
|
원자번호 70번 이터븀 <출처: NIST> |
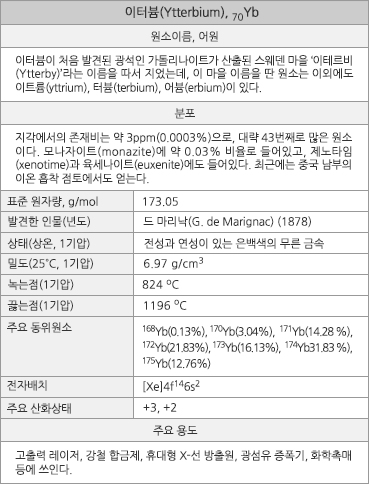
이터븀의 원소 정보 |
|
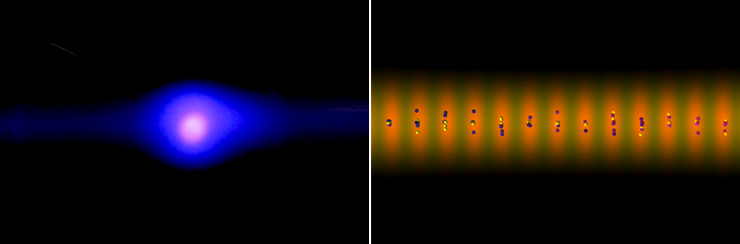
레이저 광선에 포획된 이터븀 원자 뭉치를 이용하면 차세대 원자시계인 ‘광시계’를 만들 수 있다. 왼쪽은 약 1백만개의 이터븀 원자가 격자 모양의 푸른 레이저 광선에 붙잡힌 모습. 오른쪽은 레이저에 포획된 이터븀 원자들을 높은 에너지 상태와 낮은 에너지 상태를 오가도록 노란색 레이저로 들뜨게 한 것이다. <출처: NIST>
|
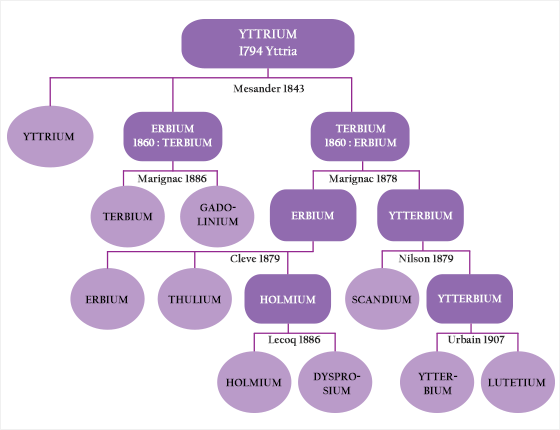
이트륨에서 출발한 희토류 원소들의 발견 계통도. 진한 색은 불순물이 많이 포함된 것이고, 옅은 색은 이들에서 분리된 비교적 순수한 원소이다. 실제로 처음 분리되어 발견된 것은 원소 자체가 아니고 이들의 산화물이었다. 드 마리낙은 모산데르가 지은 어븀과 터븀을 혼돈하여 바꾸어 불렸는데, 이렇게 뒤바뀐 이름이 지금 사용되는 이름이고 이 그림은 이를 반영하였다.
|

이터븀 금속 사진 <출처: (cc) http://images-of-elements.com/>
|
|
|
|
|
|

모나자이트. 이터븀은 주로 모나자이트에서 얻는데, 여기에 이터븀이 약 0.03%의 비율로 들어 있다. <출처: (cc) Rob Lavinsky / iRocks.com>
|

독일 표준기관(PTB)의 이터븀 광시계(부분) <출처: PTB>
|

산화이터븀(III)(Yb2O3). 이터븀은 주로 산화이트븀(III) 형태로 생산되어 판매된다.
|
 수치로 보는 이터븀
수치로 보는 이터븀이터븀의 표준원자량은 173.054g/mol이고, 원자의 바닥 상태 전자배치는 1s22s22p63s23p63d104s24p64d105s25p64f146s2([Xe]4f146s2)이며, 화합물에서 주된 산화 수는 +3이나 여러 +2가 상태의 화합물들도 고체상태에서 안정하게 존재한다. 지각에서의 존재 비는 약 3ppm(0.0003%)으로, 43번째로 풍부한 원소이다. 1기압에서 녹는점은 824oC이고 끓는점은 1196oC이며, 25oC에서의 밀도는 6.97g/cm3이고 녹는점에서의 액체 밀도는 6.21g/cm3이다. 녹음열과 증발열은 각각 7.66kJ/mol과 159kJ/mol이다, 3가지 동소체가 존재하는데, 이들 간의 전이 온도는 -13oC와 795oC이다. 실온에서의 전기전도도는 3.5x106 S m-1이다. 첫 번째, 두 번째, 세 번째 이온화 에너지는 각각 603.4, 1174.8, 2417kJ/mol이며, 폴링의 전기 음성도는 대략 1.1이다. 원자 반경은 176pm(비교: Tm, 175.9pm; Lu, 173.8pm)이며, 6배위체의 Yb3+ 이온 반경은 86.8pm(비교: Tm3+, 89.0pm; Lu3+, 86.1pm)이다. Yb3+/Yb2+와 Yb3+/Yb의 표준 환원 전위는 각각 -1.05V와 -2.22V이다. 천연상태 동위원소는 168Yb(0.13%), 170Yb(3.04%), 171Yb(14.28%), 172Yb(21.83%), 173Yb(16.13%), 174Yb(31.83%), 176Yb(12.76%)의 7가지인데, 이들은 모두 안정하다. 전세계 연간 생산량은 약 50톤이고, 광석 매장량은 약 100만 톤으로 추정된다.
발행일 2013.01.16
Ytterbium
Ytterbium has useful catalytic properties and is finding increasing use in the chemical industry due to its low toxicity and relative abundance. It is the last of four elements named after the town of Ytterby, Sweden. Scroll down to see examples of Ytterbium. | |||||||||||||||||
'Natural science > 화 학' 카테고리의 다른 글
| Hafnium(Hf), 72-하프늄 (0) | 2013.02.13 |
|---|---|
| Lutetium(Lu), 71-루테튬 (0) | 2013.01.23 |
| The Photogarphic peroidic table of the elements (0) | 2013.01.11 |
| 중국의 조주공부차(潮州功夫茶) (0) | 2013.01.09 |
| 하동녹차 (0) | 2013.01.09 |


 Yb2+ Eo = -1.05V
Yb2+ Eo = -1.05V