|
|
원자번호 98번 캘리포늄, 사진은 미국 캘리포니아주의 금문교. |
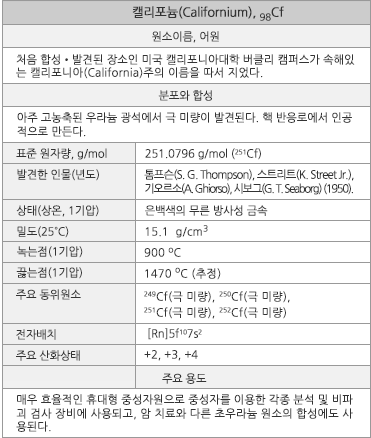
캘리포늄의 원소정보 |
|
|
물리적 성질
|
|
|
|
|
캘리포늄의 합성과 분리
|
|
|
|
|
캘리포늄-252를 중성자원으로 사용한 중성자 지뢰 탐지기. |
미국 국립표준기술연구소(NIST)의 캘리포늄 중성자 조사 시설(Californium Neutron irradiation Facility) |
|
|
|
|
|
 수치로 보는 캘리포늄
수치로 보는 캘리포늄 캘리포늄은 질량수가 237~256인 20가지 동위원소가 알려져 있는데, 가장 안정한 것은 반감기가 898년인 251Cf이며 이의 표준 원자 질량은 251.0796 g/mol이다. 실용적으로 주로 사용되는 동위원소는 반감기가 2.645 년인 252Cf인데, 이의 96.91%는 α-붕괴를 하여 248Cm이 되고, 3.09%는 자발적 핵분열을 하고 중성자를 방출한다. 1 μg의 순수한 252Cf는 1초 당 230만 개의 중성자를 방출한다. 원자의 바닥상태 전자배치는 1s22s22p63s23p63d104s24p64d105s25p64f145d106s26p65f107s2([Rn]5f107s2)이다. 미국과 러시아에서 플루토늄-239에 고선속 중성자를 장기간 쪼여 만들며, 연간 생산량은 약 0.3 g이다. 1기압에서 결정 구조가 서로 다른 α-형와 β-형의 두 가지 동소체가 있다. 녹는점은 900℃, 끓는점은 1470℃(추정)이고, 실온에서의 밀도는 15.1 g/cm3이다. 화합물에서는 +2, +3, +4의 산화상태를 갖는데, +3의 상태가 가장 안정하고 흔하다. 용액에서는 +3가 이온만 존재한다. 첫 번째와 두 번째 이온화 에너지는 각각 606 kJ/mol과 1138 kJ/mol이며, 폴링의 전기음성도는 1.3이다. 원자반경은 186 pm이고, 6배위된 Cf4+의 이온반경은 82 pm, Cf3+의 이온반경은 95 pm이다. 산성 수용액에서 Cf4+/Cf3+와 Cf3+/Cf의 표준 환원전위(Eo)는 각각 3.2 V와 -1.91 V이다.
발행일 2013.09.03
Californium
Californium is named after the state of California, home of UC Berkeley where it was discovered. It is used as a convenient portable neutron source for detection of precious metals and in oil well logging. Scroll down to see examples of Californium. | |||||||||||||||||
'Natural science > 화 학' 카테고리의 다른 글
| 주기율(periodic Law) (0) | 2014.07.05 |
|---|---|
| Einsteinium(Es), 99-아인슈타인늄 (0) | 2013.11.22 |
| Berkelium(Bk), 97-버클륨(Bk) (0) | 2013.11.22 |
| Curium(Cm), 96-퀴륨(Cm) (0) | 2013.11.22 |
| Americium(AM), 95- Am(아메리슘) (0) | 2013.11.22 |