
원자번호 108번의 원소 하슘(hassium, Hs)은 열여섯 번째 초우라늄 원소이고 다섯 번째 초악티늄족 원소(transactinide element)인데, 주기율표에서 7주기 8족에 있는 전이금속 원소이다. 1984년에 독일 중이온 가속기연구소(GSI) 연구진이 납-208에 철-58 이온을 충돌시켜 질량수가 265인 동위원소 원자 6개를 생성시켜 확인한 것이 이 원소의 처음 합성이자 발견으로 간주된다. 원소 이름은 이 연구소가 소재한 독일 헤센(Hessen)주의 중세 라틴어 이름 하시아(Hassia)를 따서 지었다. 독일(Germany)이란 나라 이름을 딴 원소로 저마늄(Ge, 원자번호 32)이 있고, 가속기연구소가 위치한 주 이름과 도시 이름을 각각 딴 원소인 하슘과 다름슈타튬(Ds, 원자번호 110번)이 있으니, 독일은 미국과 함께 국가 이름, 핵물리학 연구소가 소재한 주 이름과 도시 이름을 딴 원소가 모두 있는 나라가 되었다. 참고로, 미국의 경우는 나라 이름을 딴 원소는 아메리슘(Am)이고, 로렌스버클리 국립연구소(LBL)가 소재한 주 이름과 도시 이름을 딴 원소는 각각 캘리포늄(Cf)과 버클륨(Bk)이다. 하슘은 모든 동위원소들의 반감기가 아주 짧은 방사성 원소인데, 알려진 것들 중에서 가장 안정한 동위원소의 반감기가 약 9.7초에 불과하다. 이런 원소의 화학적 성질이 부분적이나마 실험적으로 조사되었는데, 같은 족의 오스뮴(Os)처럼 휘발성인 사산화물(HsO4)을 만드는 것이 밝혀졌다. 한편, 하슘은 이론적으로는 긴 수명의 핵 이성질체가 있을 가능성이 있어, 미래에 실용적으로 사용될 여지도 있다. 하슘의 발견, 특성, 합성 등에 대해 보다 자세히 알아보기로 하자.
원자번호 108번, 하슘
하슘(hassium)1)은 원자번호 108번의 원소로, 원소 기호는 Hs이다. 주기율표에서 d-구역의 초악티늄 원소의 하나이며, 7주기 8족에 있는 전이금속 원소이다. 8족 원소로는 철(Fe), 루테늄(Ru), 오스뮴(Os)도 있는데, 하슘은 오스뮴 바로 아래에 있으므로 에카-오스뮴(eka-osmium)이라 부를 수 있고, 화학적 성질도 오스뮴과 비슷하다.

독일 헤센(Hessen)주의 이름을 딴 원소 하슘. |
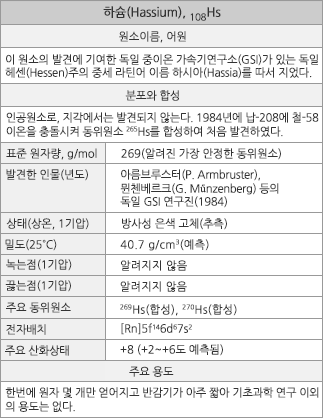
하슘의 원소정보 |
하슘은 인공 방사성 원소로, 자연에서는 발견되지 않았으며, 입자 가속기를 사용하여 보다 가벼운 원소 표적에 가속된 중(重)이온을 충돌시켜 얻거나, 보다 원자번호기 큰 원소의 α 붕괴 사슬의 생성물로 얻는다. 1984년에 독일 헤센(Hessen)주 다름슈타트(Darmstadt)에 있는 중이온 가속기연구소(Gesellschaft fűr Schwerionenforschung, GSI)에서 납-208(208Pb) 표적에 가속된 철-58(58Fe) 이온을 충돌시켜 265Hs를 생성·확인한 것이 이 원소의 처음 발견으로 간주된다. 지금까지 12가지의 동위원소와 1~4가지의 핵 이성질체가 확인되었는데, 알려진 동위원소 중 반감기가 가장 긴 것은 반감기가 약 9.7초인 269Hs이다. 그러나 아직 발견되지 않은 몇 가지 동위원소들의 반감기가 이보다 길 것으로 예측되었다. 한편, 수명이 긴 하슘 동위원소의 핵 이성질체가 일부 천연 광석에 존재할 것이라는 주장이 있었으나, 아직 이를 확인하지는 못하였다. 만약 그런 이성질체가 실제로 존재한다면, 언제가 이를 실용적으로 유용하게 사용할 수도 있을 것이다.
하슘은 한번에 단지 원자 몇 개만 만들어지는데, 지금까지 합성된 원자의 수는 100개가 조금 넘는 정도이며 반감기도 짧아 물리∙화학적 특성은 잘 알려져 있지 않다. 그러나 표준상태에서 은색 금속 고체이고, 산소와 잘 반응할 것으로 예측되었다. 밀도는 40.7 g/cm3으로 예측되며, 녹는점과 끓는점은 알려지지 않았다. 2001년에 GSI에서 몇 가지 화학적 성질이 실험적으로 연구되었는데, 오스뮴(Os)처럼 산화상태가 +8인 휘발성 사산화하슘(HsO4)을 만드는 것이 밝혀졌다. 이외 +2~+6 의 산화상태도 가능할 것으로 여겨진다.
하슘의 발견과 역사
108번 원소 하슘에 대한 관심은 1960년대 초반에 구 소련 과학자가 천연 몰리브데넘 광석에서 수명이 긴 이 원소의 동위원소를 발견하였다는 주장에서 시작되었다. 그러나 이 주장은 이후 검증되지 않았고, 108번 원소는 결국 1984년에 핵 융합 반응에 의해 처음 합성되었다. 하슘의 발견과 역사에 대해 천연 광석에서 원시(primordial) 하슘을 발견하려는 노력과 인공적으로 합성하여 발견한 과정을 나누어 소개한다.
천연 원시 하슘을 발견하려는 노력
1960년 대 초에 일부 광석에서 당시까지 알려진 방사성 동위원소들에서 방출되는 방사능으로는 설명되지 않는 방사능이 관찰되었는데, 일부 학자들은 이것이 아마도 이들 광석에 미량으로 들어있는 아주 수명이 긴 초중(超重)원소에 의한 것이라고 설명하였다. 1963년에 동위원소의 지구화학을 연구하던 구 소련의 체르딘트세프(Victor Cherdyntsev, 1912~1971)는 카자흐스탄(Kazakhstan)에서 채굴된 몰리브데나이트(molybdenite, 휘수연석)에서 질산에서 끓이면 오스뮴처럼 휘발성 산화물이 되는 특성을 보이고, 반감기가 4~5억년이며 질량수가 267인 108번 원소(지금 표현으로 267Hs)를 발견하였다고 주장하였다. (그는 또한 일부 광석 시료에서 반감기가 2.5년으로 추정되고 α 붕괴를 하는 원시 초우라늄 원소 247Cm의 존재를 주장하기도 하였다.) 그는 108번 원소의 이름을 광석을 채취한 비단길(silk road)의 고대도시 이름 세릭(Serik)을 따서 세르게늄(sergenium)으로, 그리고 원소기호는 Sg(현재는 Sg가 106번 원소 시보귬의 원소 기호임)로 할 것을 제안하기도 하였다. 그러나 그가 주장한 하슘 동위원소의 성질이 당시의 핵 물리학 지식과 부합되지 않았기 때문에 그의 천연 하슘 발견 주장은 인정받지 못했다. 이후에 초중원소가 초변형된 상태(특히 271Hs의 핵 이성질체)로 레늄이나 몰리브데넘과 함께 몰리브데늄 광석에 있다거나, 오스뮴과 함께 오스뮴 광석에 존재할 가능성이 있다는 주장이 이론적으로 제기되었다.
하슘이 자연에 미량 존재할 것이라는 여러 주장에 따라, 러시아 합동핵연구소(Joint Institute for Nuclear Research, JINR)는 2004년에 ‘자연에서 중원소 찾기(Search for Heavy Element in Nature, SHIN)’ 프로그램을 기획하고 천연 하슘을 찾아내는 실험에 착수하였다. 이 실험은 우주선에 의한 영향을 피하기 위해 지하 깊은 곳에 설치된 프랑스의 모단 지하동굴실험실(Laboratoire Souterrain de Modane, LSM)에서 수행되었는데, 지금까지 아무 발표가 없는 것으로 보아, 아직 천연 하슘을 발견하지는 못한 것으로 짐작된다. 지금까지의 결과를 종합할 때, 천연 하슘의 존재는 이론적으로는 가능하나, 아직도 붕괴되지 않고 실제로 남아 있을 가능성은 거의 없는 것으로 여겨지며, 따라서 하슘은 자연에는 존재하지 않고 인공적으로 합성되는 원소로 간주된다.

몰리브데나이트(molybdenite) 광석. 수명이 긴 하슘 동위원소 이성질체가 일부 천연 광석에 들어있고, 몰리브데나이트에서 이를 발견하였다는 주장이 있었다. 그러나 여러 노력에도 불구하고 아직 천연 하슘은 확실하게 검출되지는 않았다. 만약 수명이 긴 하슘이 실제로 존재한다면, 언젠가는 이를 실용적 목적으로 이용할 수도 있을 것이다.
핵 합성에 의한 하슘의 발견과 명명
108번 원소 하슘의 핵 합성을 위한 첫 번째 시도는 1978년에 러시아 두브나(Dubna)에 소재한 합동핵연구소(JINR)의 플레로프 핵반응연구실(FLNR)에서 이루어졌다. 오가네시안(Yuri Organessian, 1933~)이 이끄는 연구팀은 질량수 270인 동위원소(현재의 표기로 270Hs)를 얻기 위해 226Ra 표적에 가속된 48Ca 이온을, 그리고 264Hs를 얻기 위해 208Pb 표적에 58Fe 이온을 충돌시키는 실험을 수행하였는데, 그들은 실험 결과가 확실하지 않다고 여겨 논문으로 발표하지 않았다. 오가네시안 팀은 다시 1983-1984년에 하슘의 합성 실험을 수행하였는데, 이번에는 209Bi 표적에 55Mn 이온, 207Pb과 208Pb 표적에 58Fe 이온을 충돌시켰다. 그들은 209Bi/55Mn 반응에서 반감기가 약 1.9초로 자발적 핵분열을 하는 생성물을 검출하였는데, 이를 핵 융합으로 생성된 263Hs가 두 번의 α 붕괴를 일으켜 얻어진 손녀 핵종(granddaughter nuclide) 255Rf에 의한 것으로 설명하였다. 또한, 그들은 208Pb/58Fe와 207Pb/58Fe 반응에서도 모두 자발적 핵 분열을 하는 생성물을 검출하였는데, 이를 264Hs의 딸 핵종(daughter nuclide) 260Sg에 의한 것으로 설명하였으며, 후속 실험에서는 265Hs의 연속적인 방사성 붕괴 생성물인 253Es와 253Fm을 검출하였다고 보고하였다.
하슘의 확실한 합성·발견은 1984년에 독일 다름슈타트(Darmstadt)에 소재한 중이온 가속기연구소(GSI)의 아름브루스터(Peter Armbruster, 1931~)와 뮌첸베르크(Gottfried. Műnzenberg, 1940~)가 이끄는 연구팀에 의해 이루어졌다. 그들은 러시아 팀과 마찬가지로 208Pb/58Fe 반응을 수행하였는데, 중이온 반응 생성물 분리기(Separator for Heavy-Ion reaction Products, SHIP) 시설을 사용하여 질량수 265인 동위원소(265Hs) 원자 3개를 확실하게 검출하였으며, 265Hs의 α 붕괴 반감기는 1.1~4 밀리초 임을 밝혔다. 그들은 또한 이의 α 붕괴로 생성된 딸 핵종, 261Sg과 손녀 핵종, 257Rf도 검출·확인하였다고 발표하였다.

101번 이후의 다른 초페르뮴 원소들에 대해서와 마찬가지로, ‘108번 원소의 발견자로 누구를 인정할 것인가’하는 문제가 또다시 제기되었다. 이를 해결하기 위해 1985년에 국제순수·응용화학연맹(IUPAC)과 국제순수·응용물리연맹(IUPAP)은 초페르뮴 특별소위원회(TWG)를 구성하고 관련 당사자들의 주장을 검토하였다. TWG는 1993년의 최종 보고서에서 ‘108번 원소의 합성은 다름슈타트와 두브나에서 동시에 독립적으로 이루어졌으나, 다름슈타트에서의 연구가 보다 구체적이고 신빙성있게 원소를 확실하게 생성·확인하였으므로 발견에 대한 주된 공적은 다름슈타트 팀에게 주어져야 한다’고 결론지었다.
1992년에 다름슈타트의 중이온 가속기연구소(GSI) 연구자들은 108번 원소의 이름을 연구소가 소재한 헤센(Hessen)주의 중세 라틴어 이름 하시아(Hassia)를 따서 하슘(hassium)으로 할 것을 제안하였다. 반면에, IUPAC은 1994년에 독일 방사화학자 오토 한(Otto Hahn, 1879~1968: 핵 분열의 발견으로 1944년 노벨화학상을 수상하였고 ‘핵화학의 아버지’라 불린다)의 이름을 따서 하늄(hahnium, 원소기호 Hn)으로 할 것을 제안하였는데, 하늄은 같은 해에 미국화학자들에 의해 105번 원소(지금 이름은 더브늄)의 이름으로 제안되었다. 원소 발견의 주된 공적을 인정받은 GSI는 자신들의 제안을 고집하였고, 미국화학회도 1995년부터 논문에 GSI가 제안한 하슘을 사용하기 시작하였다. 마침내 1997년에 IUPAC에 의해 104~109번 원소 이름이 함께 확정될 때, 108번 원소 이름은 하슘으로 최종 결정되었다. 참고로, IUPAC이 제안했던 하늄이란 이름은 아직 어떤 다른 원소에도 사용되지 않고 있다.

독일 중이온 가속기연구소(GSI)의 중이온 반응 생성물 분리기(Separator for Heavy-Ion reaction Products, SHIP) 부분 사진. <출처: 독일 중이온 가속기연구소(GSI)>
물리적 성질
하슘은 모든 동위원소가 반감기가 아주 짧은 방사성 원소로, 한번에 원자 몇 개만 얻어지므로 물리 및 화학적 특성들은 거의 알려져 있지 않다. 그러나 몇 가지 성질들이 이론적 계산과 원소들의 주기율적 성질에서 예측되었다. 상온에서 은색 고체 금속이며, 결정은 육방밀집(hcp) 구조를 할 것으로 예측되었다. 녹는점과 끓는점은 알려지지 않았으나, 다른 8족 원소들의 녹는점과 끓는점이 아주 높은 것(예로, 오스뮴의 녹는점 3030℃, 끓는점 5012℃)에서 하슘의 녹는점과 끓는점도 아주 높을 것으로 예측된다. 밀도는 약 40.7 g/cm3로 예측되었는데, 이는 지금까지 알려진 118개 원소 중에서 가장 크다. 원자 반경은 약 126 pm로 예측되었다.
동위원소와 방사성 붕괴 성질
지금까지 알려진 하슘의 동위원소는 질량수가 263~271, 273, 275, 277인 12가지이다. 이중에서 266Hs와 질량수 273 이상인 동위원소들은 직접 합성되지는 않았으며, 보다 원자번호가 크고 짝수인 원소들의 α 붕괴 사슬에서 중간생성물로 발견되었다. 핵 이성질체는 265mHs과 266mHs가 알려져 있다. 알려진 동위원소 중에서 반감기가 가장 긴 것은 269Hs(반감기 약 9.7초)인데, 아직도 확증되지 않은 핵 이성질체 277mHs의 반감기가 11분으로 측정되어 보고되었고, 미발견된 동위원소 272Hs, 274Hs, 276Hs의 반감기가 각각 대략 40초, 1분, 1시간으로 예측되었다. 다른 여러 초페르뮴 원소들과 마찬가지로, 하슘의 반감기도 단지 검출된 원자 몇 개의 수명에서 계산된 것이므로 불확실성이 크고, 자료마다 큰 차이를 보이는 경우가 많다. 대부분의 하슘 동위원소들은 거의 전적으로 α 붕괴를 하고 시보귬(Sg) 동위원소가 된다. 다만 264Hs는 거의 같은 비율로 α 붕괴와 자발적 핵분열을 하며, 277Hs는 딸 핵종 273Sg가 발견되지 않은 것으로 보아 주로 자발적 핵 분열을 하는 것으로 여겨진다.
화학적 성질
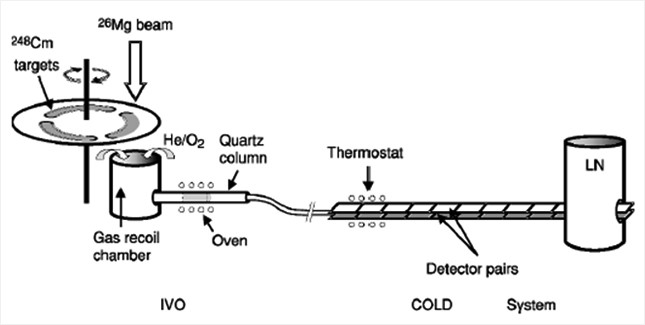
2002년에 다국적 연구진이 네이처(Nature)에 발표한 것으로, 하슘의 화학적 성질을 연구하는데 쓰인 실험장치의 모식도. 248Cm 표적에 26Mg 이온을 충돌시켜 얻은 하슘 원자를 산소와 반응시켜 휘발성 HsO4로 전환시키면 HsO4는 검출기 표면에 흡착되고, 여기서 방출되는 α 입자로 검출된다. 모두 5개의 하슘 원자를 합성·조사하였는데, 하슘은 오스뮴과 성질이 비슷한 것으로 밝혀졌다. LN은 액체질소임. <출처:http://en.wikipedia.org/wiki/Hassium>
하슘은 8족 원소로, 주기율표에서 오스뮴(Os) 바로 아래에 있다. 따라서 이의 화학적 성질은 오스뮴과 가장 비슷할 것으로 예상된다. 주된 산화상태는 +8이나, +2~+6의 산화상태를 갖는 화합물도 가능할 것으로 예상된다. 기체 상태 화학 실험에서 하슘은 산소와 반응하여 아주 휘발성이 큰 사산화하슘(HsO4)을 생성하는 것으로 나타났다. HsO4는 사산화오스뮴(OsO4, 끓는점 129.7℃)보다는 휘발성이 적으며, 검출기 표면에서의 흡착 엔탈피는 OsO4와 비슷한 것으로 나타났다. HsO4는 수산화소듐(NaOH)과 반응하여 과하슘산소듐(Na2[HsO4(OH)2]이 된다.
Hs + 2 O2 → HsO4
HsO4 + 2 NaOH → Na2[HsO4(OH)2]
하슘의 합성
다른 초중(超重)원소들과 마찬가지로, 하슘은 입자가속기를 사용하여 보다 가벼운 원소의 표적에 중(重)이온을 충돌시켜 합성되는데, 충돌하는 이온과 표적 원소는 그들의 원자번호의 합이 하슘의 원자번호(108)가 되는 것을 선택한다. 콜드퓨전(cold fusion)과 핫퓨전 방법이 모두 사용되었다. 하슘은 또한 원자번호가 보다 크고 짝수인 초중원소의 α 붕괴 사슬에서 중간생성물로도 발견된다. 하슘 동위원소는 자체의 α 붕괴, 이에 의해 생성된 딸 핵종의 확인, 후속적인 붕괴 생성물의 시간적 상관 관계와 붕괴 특성에서 검출되고 확인된다.
독일의 중이온 가속기연구소(GSI), 러시아의 합동핵연구소(JINR), 일본의 이화학연구소(RIKEN), 프랑스의 국립 대형중이온 가속기연구소(GANIL), 미국의 로렌스버클리 국립연구소(LBL), 스위스의 폴쉐르연구소(PSI) 등에서 연구되고 합성되었다.
콜드퓨전
콜드퓨전에서는 82Pb 또는 83Bi 표적에 각각 26Fe, 25Mn 이온을 충돌시켜 합성하였다. 하슘 생성이 확인된 콜드퓨전 반응들은 다음과 같다.

위 반응은 1978년에 러시아의 JINR 연구팀이 처음 연구한 반응인데, 당시에는 생성물을 확인하지 못하였고, 1984년의 재실험에서 자발적 핵분열을 하는 생성물을 검출하고 이를 264Hs의 딸 핵인 260Sg에 의한 것으로 해석하였다. 그들은 곧 이어 265Hs의 붕괴 생성물인 253Fm와 이의 전자포획 생성물인 253Es의 α 붕괴를 검출할 수 있었는데, 265Hs에서 253Fm과 253Es가 되는 과정은 다음으로 여겨진다.

독일 GSI 연구팀은 1984년에 이 반응에서 265Hs 원자 3개를 확인하였으며, 1993년에는 성능이 더욱 향상된 시설을 이용하여 265Hs 원자 75개와 264Hs 원자 2개를 검출하였고, 1997년에는 20개의 264Hs 원자를 추가적으로 검출하였다. 2000년대에는 일본 RIKEN와 프랑스의 GANIL 연구진도 이 반응에서 이들 두 가지 동위원소를 검출하였다



위 반응들은 처음에 기술한 208Pb/58Fe 반응에서 표적 또는 충돌 이온을 다른 동위원소로 바꾼 것이다. 207Pb/58Fe 반응은 러시아 JINR 연구팀이 1984년에 연구하였는데, 264Hs의 딸 핵인 260Sg의 자발적 핵분열을 관찰할 수 있었다. 또 독일의 GSI와 일본의 RIKEN 연구진도 이 반응에서 264Hs의 생성을 확인하였다. 206Pb/58Fe 반응은 일본의 RIKEN 연구진이 2008년에 연구하였는데, 그들은 이전까지 알려지지 않았던 동위원소 263Hs 원자 8개를 검출하였다. 208Pb/56Fe 반응은 미국의 LBL 연구팀이 2008년에 연구하였는데, 그들은 263Hs 원자 6개를 확인하였다.

위 반응은 1983년과 1984년에 러시아의 JINR 연구팀이 연구하였는데, 자발적 핵분열을 하는 생성물을 검출하고 이를 263Hs가 2번의 α 붕괴를 해서 생긴 255Rf로 해석하였다. 또한 262Hs가 4번의 α 붕괴를 해서 생긴 246Fm의 α 붕괴도 검출하였다고 주장하였으나, 이는 아직 검증되지 않았다.
핫퓨전
하슘 동위원소의 생성이 확인된 핫퓨전 반응들은 다음과 같다.

위 반응은 1978년에 러시아의 JINR이 처음 연구하였는데, 그 때는 결과를 발표하지 않았고, 2008년에 수행한 재실험에서 270Hs 원자 4개를 검출하였다.

위 반응은 1994년에 러시아의 JINR이 연구하였는데, 267Hs 원자 3개를 검출하였다고 발표하였다. 한편, GSI 팀은 2009년에 이 반응에서 267Hs와 268Hs 원자 각각 1개씩을 검출하였다.

위 반응은 앞의 반응에서 사용한 34S대신에 값비싼 36S를 충돌 이온으로 사용한 것으로, 2008년에 GSI에서 수행하여 270Hs 원자 1개를 검출하였는데, 270Hs와 이의 딸 핵 266Sg의 붕괴 성질이 이 실험으로 밝혀졌다.

위 반응은 2001~2005년에 독일 GSI와 스위스 PSI 공동 연구진이 연구하였는데, 이 실험 결과에서 270Hs의 반감기가 종전의 약 22초에서 3.6초로 수정되었다.
이외에 249Cf 표적에 22Ne 이온을 충돌시키는 실험이 1983년에 JINR 팀에 의해 수행되었는데, 짧은 반감기로 자발적 핵분열을 하는 여러 생성물들이 관찰되었으나, 이들이 어떤 핵 종에 의한 것인지는 구체적으로 확인되지 않았다.
보다 무거운 원소의 붕괴 생성물로 얻는 경우
하슘의 동위원소들은 보다 원자번호가 크고 짝수인 원소들이 일으키는 α 붕괴 사슬의 중간 생성물로도 검출된다. 원자번호 110번인 다름슈타튬(Ds)은 질량수가 267, 269~271, 273, 277, 279, 281인 8가지 동위원소가 알려져 있는데, 이들이 모두 α 붕괴를 하고 하슘 동위원소가 된다. 또 원자번호 112번 코페르니슘(Cn), 114번 플레오븀(Fl), 116번 리버모륨(Lv)의 동위원소들 중에서 각각 한 번, 두 번, 세 번 α 붕괴를 하여 위에 언급한 질량수의 Ds로 전환되는 것들은 이들 Ds를 거쳐 하슘 동위원소를 생성한다. 예로, 283Cn, 287Fl, 291Lv는 279Ds를 거쳐 275Hs로 붕괴된다.
![]() 수치로 보는 하슘
수치로 보는 하슘
하슘 원자의 바닥상태 전자배치는 1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p65f146d67s2([Rn]5f146d67s2)로 예상된다. 질량수가 263~271, 273, 275, 277인 12가지 동위원소가 알려져 있는데, 반감기가 가장 긴 것은 269Hs(반감기 약 9.7초)이다. 그러나 아직 확증되지는 않았으나 핵 이성질체 277mHs의 반감기가 11분으로 측정되어 보고되었고, 미발견된 동위원소 272Hs, 274Hs, 276Hs의 반감기가 각각 대략 40초, 1분, 1시간으로 예측되었다. 녹는점과 끓는점은 알려져 있지 않으며, 밀도는 40.7 g/cm3로 지금까지 알려진 원소 중에서 가장 클 것으로 예측되었다. 첫 번째, 두 번째, 세 번째 이온화 에너지는 각각 733.3, 1756, 2827 kJ/mol로 추정되었다. 주된 산화상태는 +8이나, +2~+6의 산화상태를 갖는 화합물들도 존재하리라 예상된다. 원자의 반경은 126 pm로 예측되었다.

- 글
- 박준우 이화여대 명예교수(화학)
- 서울대학교 화학과를 졸업하고 템플대학교에서 박사학위를 받았다. 오랫동안 이화여대에서 화학을 연구하고 가르쳤다. 저서로 [인간과 사회와 함께한 과학기술 발전의 발자취]와 [아나스타스가 들려주는 녹색화학 이야기] 등이 있고, 역서로 [젊은 과학도에 드리는 조언] 등이 있다.
- 저자의 책 보러가기인물정보 더보기
Hassium
Hassium is named for Hessen, the state in Germany that is home to the institute at which it was discovered. It has a half-life of a few seconds, which is to say there's never been much of it, and isn't any right...now. Scroll down to see examples of Hassium. | |||||||||||||||||
'Natural science > 화 학' 카테고리의 다른 글
| Darmstadtium(Ds), 110-다름슈타튬 (0) | 2014.07.05 |
|---|---|
| Meitnerium(Mt), 109-마이트너륨 (0) | 2014.07.05 |
| Bohrium(Bh), 107-보륨 (0) | 2014.07.05 |
| Seaborgium(Sg), 106-시보귬 (0) | 2014.07.05 |
| Dubnium(Db), 105-더브늄 (0) | 2014.07.05 |