|
|
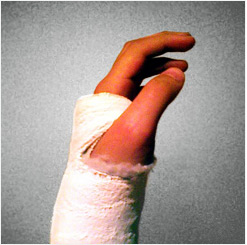
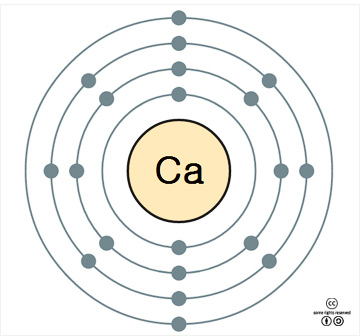
원자 번호 20번, 칼슘. <출처: sxc.hu> |
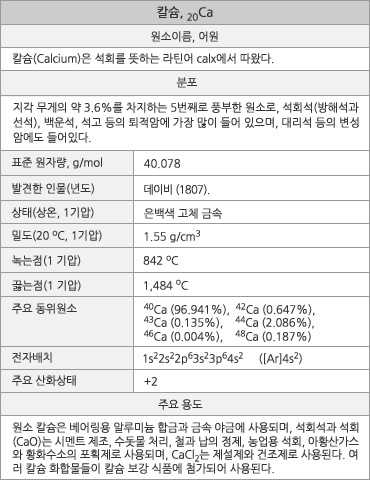
칼슘의 원소 정보. |
|
|
|
|
칼슘의 역사와 분리∙발견

|
|
물리적 성질

|
|
|
|
석회석. 석회석은 가장 흔한 칼슘 광물로, 바닷물 속에 들어있던 Ca2+와 탄산가스(CO2)가 반응해서 생겼거나, 산호나 유공충 같은 해양 생물의 껍데기나 골격이 화석화되어 만들어진 것이다. 고대부터 건축재료, 도로 건설의 기초 재료로 사용되어 왔다. |
대리석. 대리석은 석회석이나 백운석 같은 퇴적암이 변성되어 생긴 것으로, 들어있는 불순물에 따라 아름다운 무늬와 색을 띤다. 조각과 건축재료로 사용되어 왔다. <출처: (CC) Lmbuga Commons at Wikipedia.org> |
|
|
석회동굴. 석회동굴은 CaCO3가 지하수에 녹아서 만들어진 것이며, 종유석, 석순은 물에 녹은 CaCO3가 재 침전하여 만들어진 것이다.<출처: (CC)David Bunnell at Wikipedia.org> |
석회화단구. 미국 옐로스톤 국립공원의 맘모스 스프링에는 CaCO3가 녹아있는 온천수가 분출되어 흘러내리면서 CaCO3가 재 침전되어 만들어진 계단 형태의 석회화단구가 웅장한 모습으로 드러나 있다. <출처: (CC)David Monniaux at Wikipedia.org> |
|
석회석과 석회의 산업적 이용

|
|
|
|
|
|
|
|
|
|
석고를 구워서 얻는 소석고는 물과 반죽하면 굳어지기 때문에 의료용 석고붕대, 주물의 주형 등에 사용된다. |
차아염소산칼슘(Ca(OCl)2)은 수산화칼슘(Ca(OH)2)을 염소와 반응시켜 얻는데, 천의 표백, 수돗물과 수영장 물의 살균 소독, 탈취제, 곰팡이와 조류의 번식 억제제 등으로 사용된다. <출처: gettyimages> |
|
칼슘의 생물학적 역할

|
|
|
칼슘의 과잉과 결핍

|
|
- 수치로 보는 칼슘
칼슘의 표준원자량은 40.078g/mol이다. 원자의 바닥 상태 전자배치는 1s22s22p63s23p64s2 ([Ar]4s2)이며, 화합물에서의 산화 수는 +2만 있다. 지각 무게의 약 3.6%를 차지하는 5번째로 풍부한 원소이다. 1기압에서 녹는점은 842 oC이고 끓는점은 1,484 oC이다. 20 oC에서 밀도는 1.55g/cm3로, 알칼리 토금속 중에서는 가장 작다. 20 oC에서 전기비저항은 33.6nΩ∙m이다. 불꽃 반응의 색은 붉은 벽돌색이다. 첫 번째와 두 번째 이온화 에너지는 각각 589.8kJ/mol과 1145.4kJ/mol 이며, 폴링의 전기음성도는 1.00이고, 원자 반경은 197pm, 이온 반경은 100pm이다. 천연 동위원소는 6가지 인데, 40Ca(96.941%), 42Ca(0.647%), 43Ca(0.135%), 44Ca(2.086%)의 4가지는 안정하며, 46Ca(0.004%)와 48Ca(0.187%)는 방사성 동위원소이다. CaCl2의 물에 대한 용해열은 -82.8kJ/mol (발열 반응)이고, CaO의 수화열은 -63.7kJ/mol이다.
발행일 2012.01.11
Calcium
| Atomic Weight | 40.078 | |
| Density | 1.55 g/cm3 | |
| Melting Point | 842 °C | |
| Boiling Point | 1484 °C | |
| Full technical data | ||
Say calcium and most people think of chalk and bones, but in pure form it is a firm, silvery metal that reacts slowly with water to give off hydrogen gas. Pure metallic calcium has few applications and is rarely seen.
Scroll down to see examples of Calcium.
Notes on the properties of Calcium:
Specific Heat: Value given for solid phase.
Up to date, curated data provided by Mathematica's ElementData function from Wolfram Research, Inc.
'Natural science > 화 학' 카테고리의 다른 글
| 골다공증(Osteoporosis) (0) | 2012.03.01 |
|---|---|
| 이(tooth), 음식을 쪼갠다 (0) | 2012.03.01 |
| Potassium ( K ), 19-칼륨 (0) | 2012.03.01 |
| Argon ( Ar ), 18-아르곤 (0) | 2012.03.01 |
| Salt (Nacl), 소금 (0) | 2012.03.01 |






 Ca2+(
Ca2+(