|
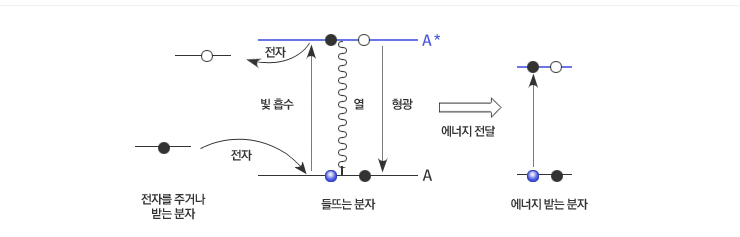
빛을 흡수한 분자에서 일어나는 분자내 및 분자간 과정. 작은 파란색 원은 들뜬 분자의 낮은 에너지 상태의 빈 자리이다.
분자의 진동 상태 때문에 형광 에너지는 흡광 에너지보다 적고, 따라서 흡수한 빛 보다 긴 파장에서 형광이 나온다.

|
|
|
|

지폐에는 위조 방지를 위해 형광 물질을 이용한 그림을 넣는다.
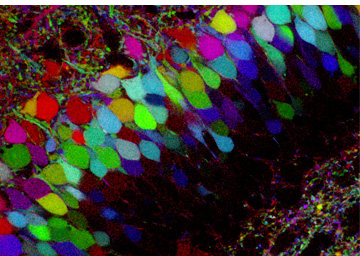
<출처: 중앙대학교 하동환 교수 연구실>

|

왼쪽부터 차례대로 시모무라, 챌피, 첸 교수

|
'Natural science > 화 학' 카테고리의 다른 글
| 금속 성질표 (0) | 2012.03.28 |
|---|---|
| 발광 ( luminescence ) (0) | 2012.03.13 |
| 빛과 색 (0) | 2012.03.13 |
| 색의 근원은? (0) | 2012.03.13 |
| Aluminium (알루미늄) -재활용이 필요한 금속 (0) | 2012.03.13 |