|

|
|
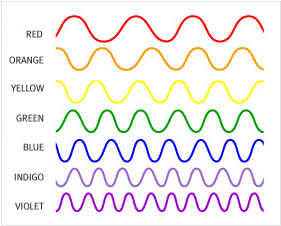
프리즘을 통해 볼 수 있는 가시 광선의 파장과 색 |
|
|

|
|

|
|
|
|
|
|
|
|
'Natural science > 화 학' 카테고리의 다른 글
| 발광 ( luminescence ) (0) | 2012.03.13 |
|---|---|
| 형광 ( fluorescent ) (0) | 2012.03.13 |
| 색의 근원은? (0) | 2012.03.13 |
| Aluminium (알루미늄) -재활용이 필요한 금속 (0) | 2012.03.13 |
| 원소주기율표 분석하기 #3/3 (0) | 2012.03.13 |