|
|
원자번호 31번, 갈륨. |
갈륨의 원소 정보. |
|
|
|
갈륨은 멘델레예프가 주기율을 통해 예언한 31번째 원소, '에카-알루미늄'이다. |
부아보드랑은 멘델레예프가 예언한 에카-알루미늄을 발견하고자 노력한 끝에 섬아연석을 처리해 갈륨을 발견한다. |
|

고순도 갈륨 결정. <출처: (CC)footbar at Wikipedia.org>
|
화학적 성질

|
|
|
갈륨의 생산

|
|
|
|
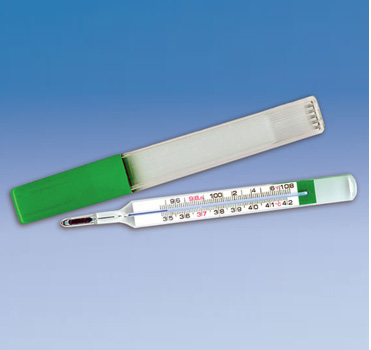
갈륨 합금인 갈린스탄은 유독성이 있는 수은을 대체한 의료용 온도계에 널리 사용된다.<출처: Geratherm> |
이탈리아의 GALLEX/GNO 검출 시설. 갈륨은 중성미자 검출 장치에도 사용된다. <출처: interactions.org> |
|
|
GaAs 등 여러 갈륨 화합물들은 발광 다이오드(LED) 제작에 쓰인다. <출처: (CC)Jeff Wilcox at wikipedia.org> |
갈륨 화합물을 이용한 다이오드 레이저가 블루레이 판독에 이용되고 있는 모습. |
|
|
-
 수치로 보는 갈륨
수치로 보는 갈륨
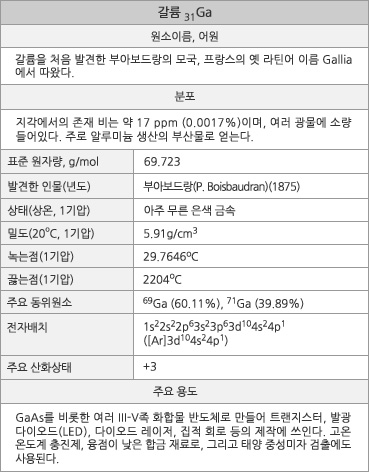
갈륨의 표준원자량은 69.723g/mol이고, 원자의 바닥 상태 전자배치는 1s22s22p63s23p63d104s24p1 ([Ar]3d104s24p1)이다. 화합물에서 주된 상태 상태는 +3이다. 지각에서의 존재 비는 약 17 ppm (0.0017%)이다. 주로 알루미늄 생산의 부산물로 얻어지며, 2009년 기준의 전 세계 갈륨 생산 시설 용량은 184톤이고, 중국이 이의 약1/3인 59톤의 생산 시설을 갖고 있다. 1기압에서 녹는점은 29.7646oC이고 끓는점은 2204oC이며, 삼중점은 29.7666oC이다. 20oC에서 밀도는 5.91g/cm3이다. 녹는점에서의 액체 밀도는 6.095g/cm3로 녹을 때 부피가 약 3.1% 줄어든다. 20oC에서 전기 비저항은 270 nΩ∙m(비교, Al 28.2 nΩ∙m)이고, 열 전도율은 40.6 W∙m-1∙K-1(비교, Al, 237 W∙m-1∙K-1)이다. 첫 번째, 두 번째, 세 번째 이온화 에너지는 각각 578.8, 1979, 2963 kJ/mol 이며, 폴링의 전기 음성도는 1.81이다. 원자 반경은 135 pm이고, Ga3+ 이온(6 배위체)의 반경은 62 pm(비교, 높은 스핀 Fe3+ 64.5 pm, 낮은 스핀 Fe2+ 61 pm)이다. 천연 상태의 동위원소는 69Ga(60.11%)와 71Ga(39.89%)로, 이들은 모두 안정하다. -
 III-V족 화합물 반도체
III-V족 화합물 반도체
IIIA족 (13족: Al, Ga, In) 원소와 VA족 (15족: N, P, As, Sb) 원소들 사이에 만들어지는 반도체 성질을 띠는 이성분 화합물들을 말한다. 대표적인 화합물들을 이들의 띠 간격 에너지(Eg)와 함께 열거하면 GaAs (Eg = 138 kJ/mol, 870 nm), GaP(Eg = 218 kJ/mol, 550 nm), GaN(Eg = 328 kJ/mol, 365 nm)이다. III-V족 화합물 반도체들을 혼합 성장시켜 다양한 띠 간격의 여러 반도체들을 얻을 수 있는데, 예로 GaAs와 GaP의 혼합 성장에서 얻어지는 GaAs1-xPx는 x값에 따라 138~218 kJ/mol (550~870 nm)의 띠 간격을 갖는다. 이들로 LED나 다이오드 레이저를 만들면 띠 간격에 해당하는 파장의 빛이 나온다. -
 발광 다이오드(Light Emitting Diode: LED)
발광 다이오드(Light Emitting Diode: LED)
전류가 흐르면 빛을 방출하는 반도체 소자로, 1962년에 홀로니악(Nick Holonyak Jr., 1928~ )이 GaAs 결정을 써서 처음 만들었다. 처음에는 여러 전자기기의 표시등과 계산기 숫자판 등으로 사용되었는데, 지금은 조명기구, LED TV의 배면 광원 등으로도 사용된다. -
 닉토겐(pnictogen)과 닉타이드(pnictide)
닉토겐(pnictogen)과 닉타이드(pnictide)
주기율표에서 15족, 즉 질소족 원소들을 닉토겐(pncitogen)이라 하며, 질소(N), 인(P), 비소(As), 안티모니(Sb), 비스무트(Bi)가 이에 속한다. 닉토겐들과 전기양성적 원소들과의 이성분 화합물을 닉타이드(pnictide)라 부르며, 대표적인 것들이 GaAs, GaN, GaP 등이다.
발행일 2012.03.28
Gallium
Atomic Weight
69.723
Density
5.904 g/cm3
Melting Point
29.76 °C
Boiling Point
2204 °C
Full technical data
Pick up gallium and it will melt in your hand: it liquefies at slightly above room temperature. A hair dryer created this Dali-esque cube. Alloys of gallium, indium and tin are replacing mercury in thermometers.
Scroll down to see examples of Gallium.
'Natural science > 화 학' 카테고리의 다른 글
| Arsenic(As), 33 - 비소 (0) | 2012.06.21 |
|---|---|
| Germanium (Ge) - 32- 저마늄 (0) | 2012.06.21 |
| Zinc(Zn), 30- 아연 (0) | 2012.04.09 |
| Copper (Cu), 29 - 구리 (0) | 2012.04.09 |
| 한국 '희토류 전쟁' 뒤늦은 노력 (0) | 2012.04.09 |