|
|
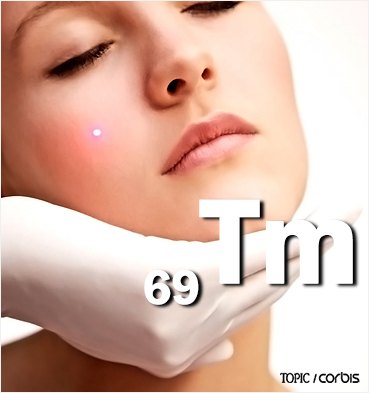
원소번호 69번 툴륨 <출처: Topic/Corbis> |
툴륨의 원소정보 |
|

휴대형 X-선 장치로 검사하는 군인의 모습
|

고순도 툴륨 입방체(왼쪽)와 금속 툴륨 (오른쪽). <출처: (CC)Alchemist-hp at Wikipedia.org>
|
|
|
|
|

툴륨은 모나자이트 광석에서 얻는데, 모나자이트에는 툴륨이 약 0.007% 비율로 들어 있다. <출처: (cc) Rob Lavinsky / iRocks.com>
|

휴대형 X-선 장치. 툴륨 동위원소 170Tm과 171Tm은 휴대형 X-선 장치의 X-선 발생원으로 사용되는데, 이들은 천연 툴륨인 169Tm에 중성자를 쪼여 만든다.
<출처: (cc) RadXman at wikimedia.org>
|
|
 수치로 보는 툴륨
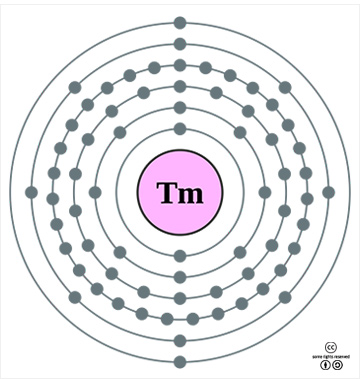
수치로 보는 툴륨툴륨의 표준원자량은 168.9342g/mol이다. 원자의 바닥 상태 전자배치는 1s22s22p63s23p63d104s24p64d105s25p64f136s2([Xe]4f136s2)이며, 화합물에서 주된 산화 수는 +3이나, +2가 상태의 화합물들도 있다. 지각에서의 존재 비는 약 0.5ppm(0.00005%)로, 루테튬과 함께 가장 희귀한 희토류 원소이다. 1기압에서 녹는점은 1545oC이고 끓는점은1950oC이며, 25oC에서의 밀도는 9.321g/cm3이고 녹는점에서의 액체 밀도는 8.56g/cm3이다. 32K 이하에서는 강자성을, 32~56K에서는 반강자성을, 그리고 56K 이상에서는 상자성을 보인다. 첫 번째, 두 번째, 세 번째 이온화 에너지는 각각 596.7, 1160, 2285kJ/mol이며, 폴링의 전기 음성도는 대략 1.25이다. 원자 반경은 175.9pm(비교: Er, 176.1pm; Yb, 176pm)이며, 6배위체의 Tm3+ 이온 반경은 88.0pm(비교: Er3+, 89.0pm; Yb3+, 86.8pm)이다. Tm3+/Tm2+와 Tm3+/Tm의 표준 환원 전위는 각각 -2.3과 -2.33V이다. 천연상태에서는 안정한 동위원소인 169Tm로만 있다. 산화물로 환산한 전세계 연간 생산량은 약 50톤이고, 광석 매장량은 약 10만 톤으로 추정된다.
 X-선 (X-Ray)
X-선 (X-Ray) 파장이 0.01~10nm인 전자파를 말하며, 주파수는 3x1016~ 3x1019Hz, 광자 에너지로는 100eV~100keV인 전자파이다. 파장이 자외선보다는 짧고(에너지가 크고) 감마선보다는 길다(에너지가 작다). X-선은 투과력이 좋으므로 물체의 내부를 투시하는데 사용되고, 과학에서는 물질 분석과 구조 결정에 X-선 형광법과 X-선 회절법이 각각 중요하게 사용된다. X-선은 보통 X-선관(진공관) 내에서 뜨거운 음극으로부터 방출되는 전자를 높은 전압으로 가속시키고 이를 금속 표적에 충돌시켜 발생시킨다. 핵의 방사성 붕괴에서 방출되는 감마선의 파장이 0.01nm보다 긴 경우는 이를 X-선이라 부르기도 하는데, 170Tm과 171Tm에서 방출되는 X-선이 그 예이다.
발행일 2013.01.09
Thulium
Thulium is among the most obscure elements in the periodic table. It has very few applications. Some people consider it the most useless of all naturally occurring elements, though others will rush to its defense. Scroll down to see examples of Thulium. | |||||||||||||||||
'Natural science > 화 학' 카테고리의 다른 글
| 생활속의 녹차 활용법 (0) | 2013.01.09 |
|---|---|
| 녹차 속 폴리페놀 (0) | 2013.01.09 |
| Erbium(Er), 68-에르븀(어븀) (0) | 2013.01.09 |
| 커피와 카페인 (0) | 2012.12.28 |
| 알카리 수 (0) | 2012.12.28 |


 Tm2+ Eo
Tm2+ Eo