
화학을 공부하는 사람들은 거의 예외 없이 원소의 주기율표(줄여 주기율표)를 접하게 된다. 주기율표는 원소들을 원자번호 순서대로 열거하되 반복되는 주기적 화학적 성질에 따라 배열한 표이다. 원소는 세상 만물을 이루는 기본 순물질로, 현재로는 자연계에 존재하는 98가지(이중 8가지는 인공적으로 합성되어 처음 발견되었으나, 자연에도 극 미량 존재한다)와 순전히 인공적으로 합성된 20가지를 합쳐 118가지가 알려져 있다. 원소들은 원자핵의 양성자 수(초기에는 원자량의 크기 순서)로 번호(원자번호)가 매겨져 있으며, 알파벳 한 개 또는 두 개의 글자로 된 기호(원소기호)로 나타낸다. 주기율표는 러시아 화학자인 멘델레예프(Dmitri Mendeleev, 1834~1907)가 1869년에 처음 만든 것으로 인정되고 있는데, 그 이전에도 원소들의 주기적 성질을 나타내는 여러 가지 표가 만들어지기는 하였으나, 멘델레예프만이 여러 원소들의 보고된 원자량을 원소 성질을 바탕으로 바르게 수정하기도 하면서 주기율표를 만들었을 뿐만 아니라, 당시에 알려지지 않은 여러 원소들에 대해서도 그 성질을 정확하게 예언하였기 때문이다. 오늘날 우리는 어떤 원소의 성질을 주기율표에 있는 그 원소의 위치로부터 거의 정확하게 예측할 수 있는데, 이것이 화학에서 주기율표를 중시하는 이유이다. 멘델레예프의 주기율표는 이후 더욱 발전된 형태로 수정·변형되어 사용되고 있다. 이번 화학산책에서는 주기율표의 역사, 주기율표의 구성, 주기율표를 바탕으로 한 원소들의 분류를 소개하며, 원소 성질의 주기성(주기율)은 글쓴이의 다음 화학산책에서 소개할 예정이다.
주기율표의 역사
주기율표의 역사에 대해서는 멘델레예프 이전에 만들어졌던 원소들의 체계화와 주기율표, 멘델레예프의 주기율표, 그리고 이후의 변형으로 나누어 소개한다.
19세기 초에 이르러서는 많은 물질들이 원소임이 확인되고 이들의 성질과 상대적 원자량이 밝혀지면서, 여러 과학자들이 원소들의 성질과 원자량 사이의 연관성을 찾으려고 시도하였는데, 이런 시도를 맨 처음 한 사람이 독일 화학자 되베라이너(Johann Wolfgang DÖbereiner, 1780~1849)이다. 그는 1828년에 화학적 성질이 비슷한 3가지 원소의 묶음들을 찾아내고는 이들을 ‘3개조(triad)’라 불렀는데, 이들의 예는 아래와 같다.
• 염소(Cl), 브로민(Br), 아이오딘(I); • 리튬(Li), 소듐(Na), 포타슘(K)
• 칼슘(Ca), 스트론튬(Sr), 바륨(Ba); • 인(P), 비소(As), 안티모니(Sb)
• 황(S), 셀레늄(Se), 텔루륨(Te)
그는 각 3개조에서, 가운데 원소의 원자량이 다른 두 원소의 원자량 평균과 거의 정확하게 같음을 발견하였다. 그러나 대부분의 사람들은 이러한 관계가 우연일 뿐이라고 여겼는데, 이런 견해는 지금도 마찬가지이다. 다만 각 3개조 원소들은 현재의 주기율표에서 같은 족(아래 참조)에 차례로 위치한다.
원자량에 따른 원소 성질의 주기성을 처음 인지한 사람은 프랑스 지질학자 샹쿠르투아(Alexander-Émile Béguyer de Chancourtois, 1820~1886)로 여겨지는데, 그는 1863년에 원소들을 원자량 순서로 원통 상에 나선형으로 배열하면 비슷한 성질을 갖는 원소들이 수직선 상에 정렬되는 것을 보이는 논문을 발표하였다. 1864년에는 독일 화학자 마이어(Julius Lothar Meyer, 1830~1895)가 49가지 원소들을 원자가(valence, 어떤 한 원자가 다른 원자와 형성하는 최대 결합수)에 따라 배열하는 표를 만들었는데, 같은 원자가를 갖는 원소들이 대체로 비슷한 성질을 보이고 되베라이너의 3개조에서의 원자량 관계가 다른 3개조들에서도 성립됨을 보였다. 그는 1868년에는 1864년에 만든 표를 개선하고, 원소들의 원자 부피가 원자량에 따라 주기적으로 변함을 보였으며, 멘델레예프가 주기율표를 발표한 몇 개월 후에는 자신의 이전 주기율표를 더욱 개선하고 확대시켜 멘델레예프의 주기율표와 매우 유사한 것을 만들었다. 또한 영국 화학자 오들링(Wiliam Odling, 1829~1921)도 1864년에 57가지 원소들을 원자량 순으로 배열하여 원소 성질의 주기성을 보이는 표를 발표하였다.
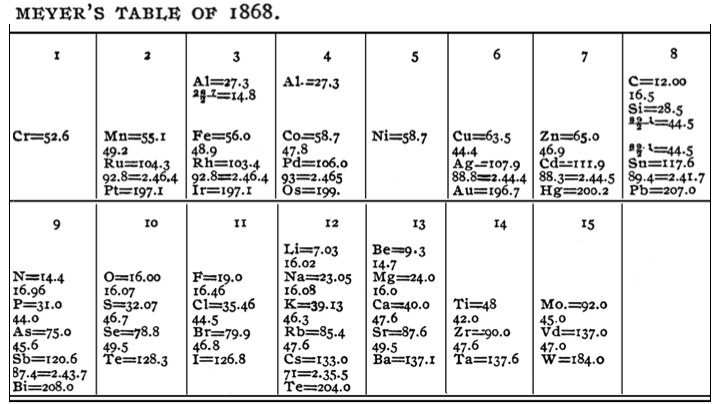
마이어(Meyer)의 1868년 주기율표. 마이어는 53가지 원소가 들어간 표를 만들어 자신이 저술한 교과서에 포함시키려 하였으나, 출판사의 실수로 빠져 이 표는 그의 생전에는 알려지지 않았다. 원소와 원소 사이에 숫자만 있는 것은 위 원소와 아래 원소의 원자량 차이이다.
영국 화학자 뉴랜즈(John Newlands, 1837~1898)는 1864년에 런던화학회 모임에서 ‘옥타브 법칙(The Law of Octaves)’이란 제목의 논문을 발표하였는데, 그는 이 논문에서 원소들을 원자량 순서로 배열하면 8의 간격으로 비슷한 성질의 원소가 반복된다는 것을 지적하였다. 그는 이를 음악에서의 8도 음정(옥타브, octave)과 비유하여 논문 제목을 선택한 것인데, 학회 회원들은 ‘알파벳 순서로 배열하는 것도 생각해 보았는가?’하는 질문 등으로 이를 비웃었다. ‘옥타브 법칙’은 학회지에 게재되는 것이 거절되었으나, 그가 이듬해에 ‘화학소식(Chemical News)'에 글을 발표하여 56개 원소들을 배열한 뉴랜즈의 주기율표는 기록으로 남게 되었다. 뉴랜즈는 이후 너무 실망하여 과학 연구를 영원히 그만 두었는데, 그의 주기율표는 바른 방향이었고, 이에 포함된 몇 가지 원소 족들은 현대 주기율표에도 들어있다. 영국화학회는 멘델레예프의 주기율표를 받아들인 5년 후에 뉴랜즈 업적의 중요성을 인식하고 그에게 금메달을 수여하였으며, 2008년에는 그가 태어난 집에 그의 이름과 ‘화학 원소들의 주기성을 발견한 사람’이라는 내용이 적힌 청색 패를 달아 그의 업적에 경의를 표했다.
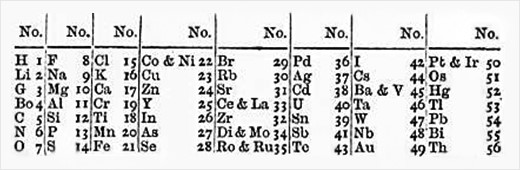
‘옥타브 법칙’을 보인 뉴랜즈의 주기율표(1865년). 숫자는 원자량 크기 순서이다.
오늘날 우리가 사용하는 것과 유사한 주기율표는 1869년에 러시아 화학자 멘델레예프가 만든 것이다. 그는 1869년 3월 6일에 열린 러시아화학회 모임에서 ‘원소의 성질과 원자량의 상관관계’라는 제목의 논문을 발표하였는데, 여기서 ‘원소 체계의 개요’란 제목의 표를 제시하였다. 구두 발표 후, 이 발표 내용을 담은 논문을 처음에는 러시아 화학회지에 게재하였는데, 뒤에 독일 학술지(Zeitschrift für Chemie)에 다시 발표함으로써 러시아 이외의 지역에도 알려지게 되었다. 이 표에는 몇 개의 의문표(?)가 들어있는데, 이는 당시까지 발견되지 않은 원소이거나, 기존에 알려진 원자량이 의문시되는 것들을 나타낸 것이다.

멘델레예프와 그가 1869년에 처음 발표한 주기율표. 숫자는 해당 원소의 원자량이다. 그는 여러 원소들의 원자량과 성질을 정확하게 예측하여 화학을 예측 가능한 학문으로 발전하게 하였다.
멘델레예프는 2년 후인 1871년에 새롭게 바꾼 주기율표를 독일어로 발표하였다. 새로운 주기율표에서는 이전의 주기율표의 가로와 세로를 바꾸었으며(이후의 화학자들은 이 모양을 따랐다), 비슷한 성질을 갖는 원소들로 구성된 세로 기둥을 족(group, 독일어로 Gruppe)이라 부르고 해당 족 원소가 만드는 산화물과 수소화물의 화학식(화학식에 있는 원자의 수는 당시 형식에 따라 위 첨자로 표기하였음)을 족 번호 바로 아래에 적었다. 또한, 1869년에 만든 주기율표에서는 단지 베릴륨(Be)와 텔루륨(Te)에 대해서만 기존의 원자량을 새롭게 바꾸었으나, 이번에는 17가지나 더 변경하였는데, 토륨(Th)과 우라늄(U)의 원자량을 각각 118에서 231로, 그리고 116에서 240으로 변경하였다. 또 존재할 것으로 예상되나 아직 발견되지 않은 여러 원소들을 ‘-’로 표시하였는데, 이중에는 우라늄보다도 원자량이 큰 초우라늄 원소도 5가지가 포함되었다. 존재를 예측한 원소들 중에서 4가지 원소들에 대해서는 그들의 원자량과 성질을 예측하였다.
앞서 언급하였듯이, 멘델레예프 이전에도 여러 사람들이 주기율표를 만들어 발표하였으나 멘델레예프를 주기율표를 처음 만든 사람으로 간주하고 그를 칭송하는 것에 대해서는 크게 두 가지 이유가 있다. 그 첫째는 멘델레예프는 원소들의 성질에 근거하여 여러 원소들에 대해 기존의 알려진 원자량이 잘못되었다는 것을 인지하고 이를 고쳐 원소들을 정확하게 주기율표상의 바른 자리에 넣은 것이다. 예로, 베릴륨(Be)은 알루미늄과 성질이 비슷하다고 하여 원자가를 3으로 여겨 당량(=원자량/원자가)을 4.6, 원자량을 13.8로 해서 원자량 순서가 탄소(C)와 질소(N) 사이에 있다고 여겨져 왔는데, 그는 원자가를 2로 하여 원자량을 9.4로 계산하고 리튬(Li)과 붕소(B) 사이에 이 원소를 넣었다. 또 텔루륨(Te)의 원자량은 기존에 알려진 128이 될 수 없다고 보고 126로 예상하여 이를 아이오딘(I, 표에는 J로 표기) 앞에 두었다(아래 참조). 또 금(Au)과 백금(Pt), 코발트(Co)와 니켈(Ni)의 순서도 바꾸었다. 멘델레예프가 이렇게 변경한 이들 원자량과 원소 순서는 텔루륨의 원자량을 제외하고는 모두 옳은 것으로 후에 밝혀졌다.
두 번째 이유는 그는 아직 발견되지 않은 원소들을 빈자리로 두었는데, 이중 4 가지에 대해서는 원자량은 물론 이들 원소와 화합물의 성질을 정확히 예언하였다. 알려져 있지 않은 원소에 대해 그 존재를 예언하고 그 성질까지 예언을 한 것은 전례가 없는 것으로 참으로 획기적이다. 멘델레예프가 예언한 원소들은 에카-붕소(eka-boron), 에카-알루미늄(eka-aluminum), 에카-망가니즈(eka-manganese), 에카-규소(ekasilicon)인데, 에카(eka)는 산스크리트어(Sanskritt)로 1을 뜻하며, 원소 에카-A는 주기율표에서 원소 A의 바로 아래에 들어갈 원소를 뜻한다. 이들 예언된 원소들은 뒤에 실제로 발견되어 각각 스칸듐(Sc), 갈륨(Ga), 테크네튬(Tc), 저마늄(Ge)으로 명명되었으며, 이들의 성질은 예측된 것과 매우 잘 일치하였다. 멘델레예프의 원소에 대한 이러한 예언은 과학에서 가장 중요시되는 ‘예측 가능성’을 보여준 것으로, 그의 주기율표로 인해 화학은 비로소 예측 가능한 진정한 과학으로 도약하게 되었다고 볼 수 있다. 아래는 멘델레예프가 예측한 에카-알루미늄(Ea)의 성질과 실제 발견해서 측정한 갈륨(Ga, 1875년에 발견)의 성질을 비교해서 보여준다.
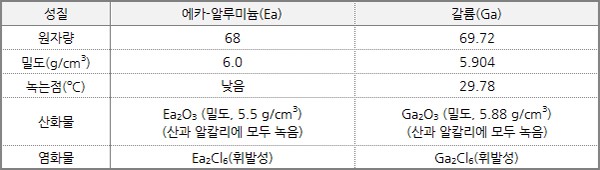
에카-알루미늄의 예측된 성질과 갈륨의 실제 성질의 비교표.
멘델레예프의 주기율표에는 비활성 기체족이 들어가 있지 않으며, 따라서 그 존재를 예측할 수도 없었다. 비활성 기체 원소들은 영국의 램지(Wiliam Ramsay)가 1894~1898년에 공기에서 분리하여 처음 발견하였는데(헬륨은 이보다 앞선 1869년에 태양 스펙트럼에서 그 존재가 확인되었고 우라늄 광석에 포획된 기체에서 실제로 분리·확인되었다), 그는 기존 주기율표를 변경시키지 않고 0족을 추가하여 이들 원소들을 배치하였다.
1900년대 초반에는 원자 구조가 밝혀지면서, 원소들을 원자량(A) 순서가 아니고 핵의 양성자 수(원자번호, Z) 순으로 배열하여야 한다는 생각이 대두되었다. 1914년에 모즐리(Henry Moseley)는 각 원소의 고유 X-선 파장과 원자번호 사이의 상관관계를 발견하고, 각 원자의 원자번호를 결정하였다. 이에 따라 원소들을 원자량 순서가 아닌 원자번호 순서로 배열할 수 있게 되었는데, 원자량 순서와 원자번호 순서가 다른 것은 아르곤(Ar: Z=18, A=39.95)과 포타슘(K; Z=19, A=39.10), 코발트(Z=27, A=58.93)와 니켈(Z=28, A=58.69), 텔루륨(Z=52, A=127.6)과 아이오딘(Z=53, A=126.9)의 3가지 경우이다. 멘델레예프는 아르곤의 존재는 예상하지 못하였으며, 다른 두 쌍은 화학적 성질에 근거하여 바르게 순서를 매겼는데, 텔루륨을 아이오딘 앞에 두기 위해 텔루륨의 원자량을 실제보다 작은 값으로 매기는 기지를 발휘하기도 하였다. 모즐리는 원자번호 43과 61인 원소들이 당시까지 발견되지 않았음을 보였는데, 43번 원소는 멘델레예프가 에카-망가니즈라 부른 테크네튬(Tc)으로 1937년에 발견되었고, 61번 프로메튬(Pm)은 1945년에 인공적으로 합성되어 발견되었다.
오늘날 사용되는 주기율표는 멘델레예프 식의 단(short)주기형이 아니고 18개의 세로 기둥(족)을 갖는 장(long)주기형이다. 장주기형 주기율표는 1923년에 데밍(Horace Groves Deming)이 발표한 것인데, 이후 널리 사용되어 이제는 표준형이 되었다. 이 주기율표에서는 란타넘족(계열) 원소(원자번호 57~71)들을 표 아래에 둔다. 이 후, 시보그(Glenn Seaborg)가 악티늄족 원소들을 발견하고 1945년에 이들을 주기율표 아래의 란타넘족 원소 밑에 두는 것을 제안하여 채택됨으로써 현재의 주기율표가 되었으며, 여기에는 지금까지 발견된 118번 원소까지가 모두 배치된다. 119번 이후의 원소들을 포함시키기 위해서는 기존의 주기율표가 확장되어야 하는데, 이는 네이버캐스트 ‘119번 이후의 원소’에 소개하였다.
주기율표는 이 글에서 보여준 것 외에 약 700가지의 서로 다른 형태가 제안되었는데, 그 예의 하나로 나선형 주기율표를 아래에 보였다. 국제순수·응용화학연맹(IUPAC)과 대한화학회가 채택하고 있는 주기율표는 이 글의 맨 아래 보인 것으로, 이 주기율표와 관련된 내용을 다음에 소개한다.
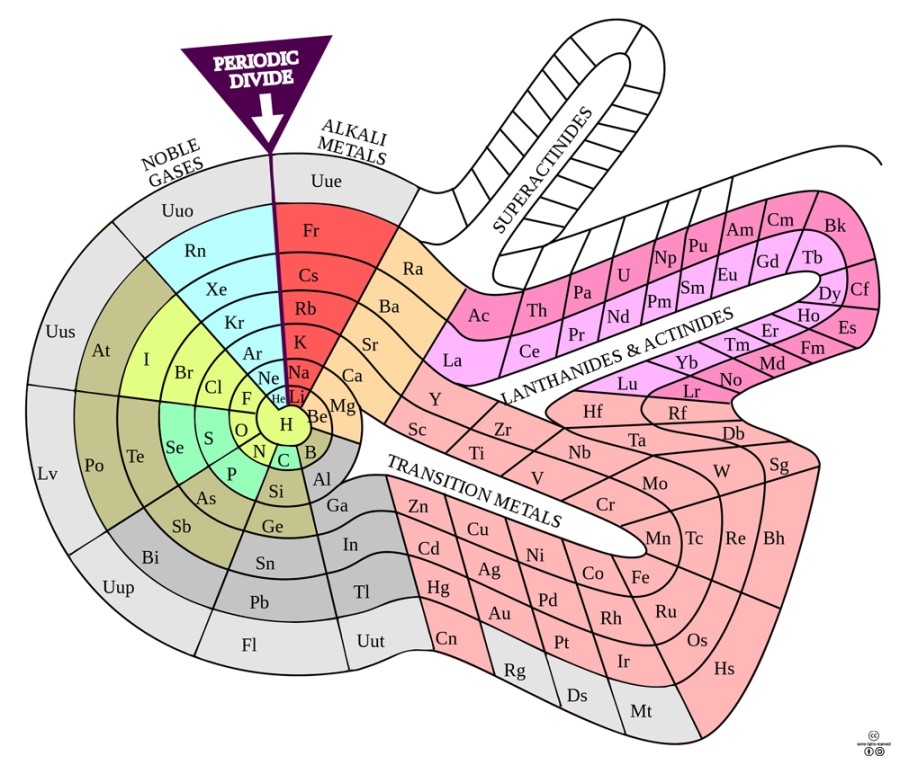
1960년에 벤파이(Theodor Benfey)가 제안하여 한때 인기를 끌었던 나선형 주기율표. 수소가 중앙에 있고, 전이금속, 란타넘족 원소, 악티늄족 원소들이 반도로 표시되어 있다. <출처 : (cc) DePiep at Wikimedia.org>
주기율표의 구성
주기율표는 원소들을 원자번호(초기에는 원자량) 순서로 배열하되, 성질이 비슷한 원소가 나오면 줄을 바꾸어 같은 열의 바로 아래 오도록 배치한 것이다. 원소의 성질은 원자의 전자배치, 특히 최외각 전자의 궤도(orbital)와 거기에 들어있는 전자의 수에 따라 결정된다. 바닥 상태 원자의 전자들은 전자배치 원리(aufbau principle) 또는 마델룽 규칙(Madelung rule)에 따라 1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p<8s<5g의 순으로 배치된다. s, p, d, f 궤도에는 각각 2, 6, 10, 14개의 전자가 들어갈 수 있다. 이에 대한 구체적 내용은 네이버캐스트 ‘원소와 원자’에 소개되었다.
주기율표에서 가로줄을 주기라 하고 위에서 아래로 1에서 7까지 번호를 매긴다. 1주기 원소는 원자번호가 각각 1과 2인 H와 He의 2가지이며 1s 전자 궤도가 채워진다. 2주기와 3주기에는 각각 8가지 원소들이 있는데, 2주기에서는 2s와 2p 궤도가, 그리고 3주기에서는 3s와 3p 궤도가 채워진다. 4주기와 5주기에는 각각 18가지 원소들이 있는데, 4주기에서는 4s, 3d, 4p전자가 채워지고, 5주기에서는 5s, 4d, 5p 전자가 채워진다. 6주기와 7주기에는 각각 32가지 원소들이 있는데, 6주기에서는 6s, 4f, 5d, 6p전자가, 그리고 7주기에서는 7s, 5f, 6d, 7p전자가 채워진다. 만약 119번 이후의 원소가 합성되거나 발견된다면, 이들에는 8s<5g 순으로 전자가 채워질 것이 예상되며, 주기율표에는 8주기 이후의 주기가 더해져서 주기율표가 더욱 확장될 것이다.
주기율표에서 세로줄(세로 기둥)을 족이라 하고 왼쪽에서 오른쪽으로 1에서 18까지 번호를 매기는데, 이는 IUPAC이 1988년에 채택한 것이다. 이전에는 단주기형 주기율표의 족 번호를 로마자로 적고 A 또는 B를 붙여, 지금의 1족과 2족은 각각 IA와 IIA로, 3~7족은 IIIB~VIIB로, 8~10족은 합쳐 VIIIB로, 11족과 12족은 각각 IB와 IIB로, 13~18족은 각각 IIIA~VIIIA로 나타내었다. 이와는 달리, 유럽에서는 지금의 1~7족을 각각 IA~VIIA, 8~10족은 합쳐 VIII, 11~17족을 각각 IB~VIIB, 그리고 18족은 0족으로 나타내기도 하였다.
한편, 주기율표에서 수소(H)와 헬륨(He)의 위치가 가끔 문제가 되기도 하였다. 다른 1족 원소들과 마찬가지로 수소는 1개의 s(1s1) 전자를 최외각에 가지나, 성질은 다른 1족 원소와 크게 달라서 가끔은 성질이 서로 약간 비슷한 플루오린(F)이나 탄소(C) 위에 두거나, 아니면 별도로 배치하기도 하였다. 헬륨은 다른 18족 원소와 같은 성질을 보이나, 전자배치가 1s2로 2족 원소의 최외각 전자배치 ns2와 같아 베릴륨(Be) 위에 두기도 하였다.
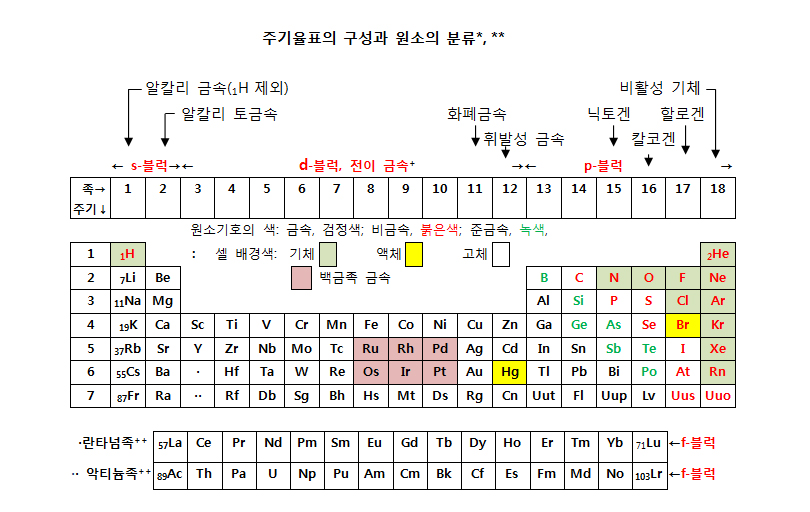
각 족의 원소들을 맨 위에 있는 원소(1족은 Li)의 이름을 따서 부르기도 함. +전이금속을 제외한 1, 2, 13~18족 원소들을 주족 원소 또는 전형 원소라 함. +12족 원소들을 주족(전형)원소로 분류하기도 함. ++란타넘족 원소들과 악티늄족 원소들을 내부전이금속이라 하는데, 문헌에 따라서는 57La과 89Ac를 3족에 포함시키고 란타넘족과 악티늄족에서는 이들을 제외시키기도 하며, 71Lu와 103Lr을 그렇게 하기도 함.
원소들의 분류
원소들을 분류하는 방법은 여러 가지가 있다. 1기압 상온에서의 상태에 따라, 기체(H, N, O. F, Cl 및 18족 원소), 액체(Br과 Hg), 고체(나머지 원소) 원소로 나누기도 하며, 전기전도성에 따라 금속, 준금속(metalloid), 비금속으로 나누기도 한다. 이외 원자의 전자배치에 따라 아래와 같이 여러 가지로 분류하기도 한다.
3~12족 원소들을 전이금속(transition metal) 원소라 부르고, 다른 족 원소들을 주족(主族, main-group) 원소라 부른다. 주족 원소들은 지구나 태양계에 풍부하게 존재하는 원소(일부 가벼운 전이금속 원소들도 많이 존재하기는 함)이므로 전형(典型, representative) 원소라 부르기도 한다. 가끔 12족 원소(Zn, Cu, Hg)들을 전이금속이 아닌 주족 원소에 포함시키기도 하는데, IUPAC의 정의에 따르면 이것이 타당하다고 볼 수 있다. 즉, IUPAC은 전이금속을 ‘원자가 부분적으로 채워진 d-부껍질을 가졌거나 부분적으로 채워진 d-부껍질을 갖는 양이온이 될 수 있는 원소’로 정의하는데, 12족 원소들의 외각 전자배치는 nd10(n+1)s2이고, 이들의 양이온은 보통 (n+1)s2 전자만 잃고 d-부껍질은 채워져 있기 때문이다. 한편, 원자나 양이온에서 부분적으로 채워진 d-부껍질을 갖는 란타넘(La)을 제외한 란타넘족 원소(lanthanides)와 악티늄(Ac)를 제외한 악티늄족 원소(actinides)들도 위의 정의로는 전이금속이 아니나, 내부전이금속(inner transition metal)으로 분류한다.
원소들을 원자의 최외각 전자의 궤도 유형에 따라 s, p, d, f-구역(block) 원소들로 분류하기도 한다. 1족과 2족 원소들은 s-구역 원소들이고, 13~18족 원소들은 p-구역 원소들이다. 그리고 전이 금속들은 d-구역 원소들이고, 란타넘족과 악티늄족 원소들은 f-구역 원소들이다.
각 족의 원소들은 해당 족의 첫 번째 원소 이름을 따서 xxx족 원소라 부르기도 하는데, 예로, 2족은 베릴륨족이고, 8족은 철족이며, 14족은 탄소족이고 16족은 산소족이다. 다만 1족은 수소족이 아닌 리튬족이라 부르고, 18족은 네온족이라고도 부른다. 그러나 보통은 전이금속 원소를 제외한 여러 족들의 원소들을 통용명으로 부르는데, 이들은 다음과 같다.
· 알칼리 금속(alkaline metal): 수소를 제외한 1족 원소들로, 반응성이 크고 이온 화합물들을 만든다.
· 알칼리 토금속(alkaline earth metal): 2족 원소들로, 알칼리 금속과 성질이 유사하나 지각에 많이 존재하기 때문에 붙여진 이름이다.
· 화폐 금속(coinage metal): 11족 원소들로 보통 뢴트게늄(Rg)을 제외하는데, 구리, 은, 금이 화폐 주조에 널리 사용되었기 때문에 붙여진 이름이다.
· 휘발성 금속(volatile metal): 12족 원소들로, 휘발성이 크기 때문에 붙여진 이름인데, 휘발성이 큰 다른 족 금속 원소들도 휘발성 금속에 포함시킬 수 있다.
· 닉토겐(pnictogen): 15족(질소족) 원소의 다른 이름이며, 반도체 성질을 갖는 2성분 화합물을 만든다.
· 칼코겐(chalcogen): 16족(산소족) 원소의 다른 이름이며, 산소를 포함시키지 않기도 한다.
· 할로겐(halogen): 17족 원소들로. 금속과 반응하여 식염(그리스어로 háls)과 비슷한 화합물을 만들기 때문에 붙여진 이름이다.
· 비활성 기체(noble gase): 18족 원소들로, 화학 반응성이 없는(현재는 일부 화합물이 발견되었음) 기체이기 때문에 붙여진 이름이다.
이들 외에 13족(붕소족) 원소들을 아이코사겐(icosagen). 14족(탄소족) 원소들을 크리스탈로겐(crystallogen)으로 부르기도 하였다.
5주기와 6주기에 있는 8~10족의 6가지 원소 루테늄(Ru), 로듐(Rh), 팔라듐(Pd), 오스뮴(Os), 이리듐(Ir), 백금(Pt)을 백금족 금속(platinum-group metal, PGMS 또는 platinoid)이라 부르는데, 이들이 성질이 비슷하고 보통 같은 광석에 함께 들어있기 때문에 붙여진 이름이다. 한편, 원자번호 92번 우라늄(U) 다음의 원소들을 초우라늄(transuranium) 원소라 부르는데, 이들이 발견 당시에 자연계에는 존재하지 않았고 인공적으로 합성되었기 때문에 다른 원소들과 구분하여 붙여진 이름이다. 또한, 100번 페르뮴(Fm) 다음의 원소들을 초페르뮴 원소 또는 초중원소(超重, superheavy)원소라 부르기도 하며, 원자번호 104번 러더포듐(Rf) 이후의 원소들은 악티늄족 원소의 마지막인 원자번호 103번 로렌슘(Lr) 다음에 있기 때문에 초악티늄족(tranactinide) 원소라 부르기도 한다.
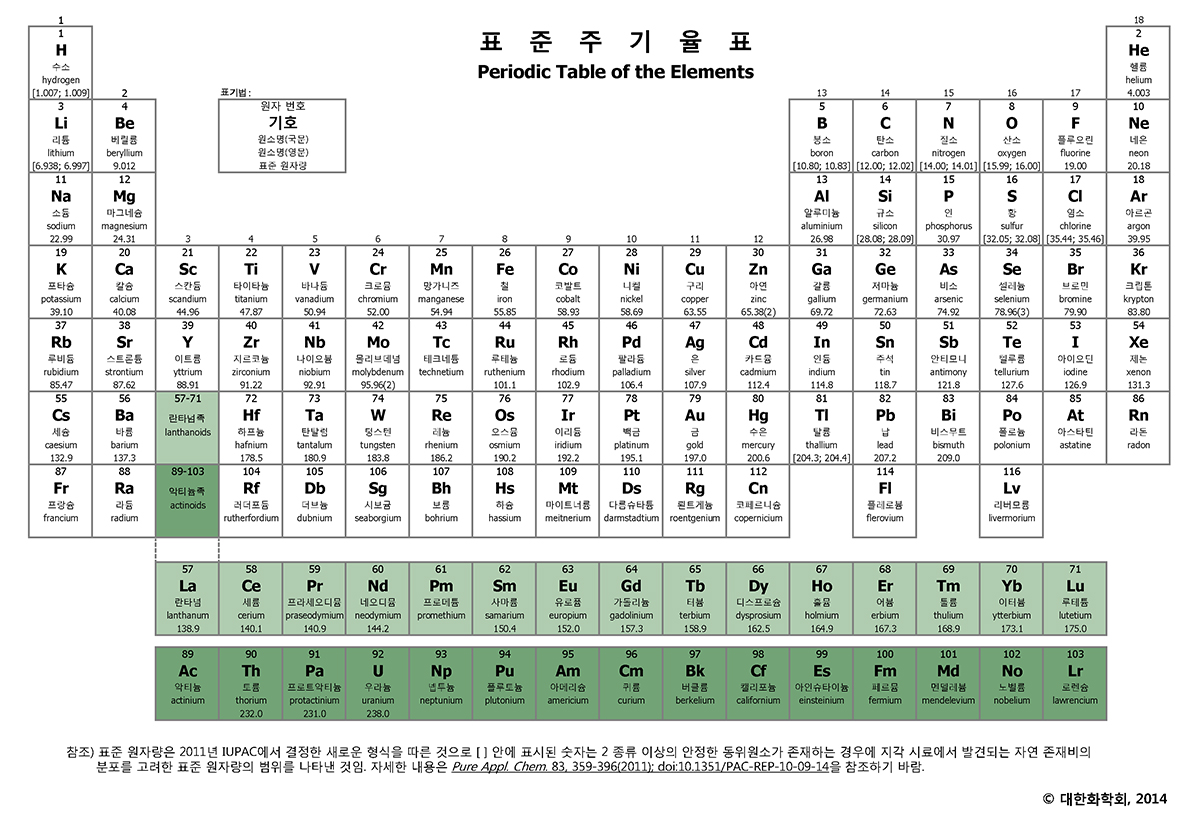
대한화학회 표준 주기율표. 118개의 원소 중 원소 발견이 아직 공식 인정되지 않은 원자번호 113번(우눈트륨, Uut), 115번(우눈펜튬, Uup), 117번(우눈셉튬, Uus), 118번(우눈옥튬, Uuo) 원소들은 이 표에 빠져있다.<출처 : 대한화학회>

- 글
- 박준우 이화여대 명예교수(화학)
- 서울대학교 화학과를 졸업하고 템플대학교에서 박사학위를 받았다. 오랫동안 이화여대에서 화학을 연구하고 가르쳤다. 저서로 [인간과 사회와 함께한 과학기술 발전의 발자취]와 [아나스타스가 들려주는 녹색화학 이야기] 등이 있고, 역서로 [젊은 과학도에 드리는 조언] 등이 있다.
- 저자의 책 보러가기인물정보 더보기
'Natural science > 화 학' 카테고리의 다른 글
| Mendelevium(Md), 101-멘델레븀 (0) | 2014.07.05 |
|---|---|
| Fermminum(Fm), 100-페르뮴 (0) | 2014.07.05 |
| 주기율(periodic Law) (0) | 2014.07.05 |
| Einsteinium(Es), 99-아인슈타인늄 (0) | 2013.11.22 |
| Californium(Cf),98- 캘리포늄(Cf) (0) | 2013.11.22 |


