|
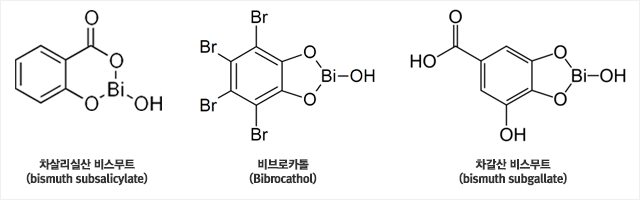
비스무트 화합물

비스무트는 산화상태가 +3과 +5인 화합물들을 주로 만드는데, +3가 상태의 화합물들이 보다 흔하다. 비소나 안티모니 화합물들과 화학적 성질이 비슷하나, 독성은 훨씬 적다. 주요 화합물로는 산화물, 칼로겐화물, 할로겐화물 등이 있다.
산화물
비스무트의 산화물은 삼산화 비스무트(Bi2O3), 사산화 비스무트(Bi2O4), 오산화 비스무트(Bi2O5)가 있다. Bi2O3는 노란색 고체로, 750~800oC에서 비스무트 금속 증기와 산소를 반응시키면 생성되는데, 상업적으로는 비스무트를 뜨거운 질산(HNO3)에 녹여 차질산 비스무트(bismuth subnitrate)를 얻은 후 여기에 과량의 가성소다(NaOH)를 넣고 가열하여 얻는다. 실온에서 안정한 결정형은 단사정(monoclinic)계의 α-Bi2O3인데, 이는 729oC에서 면심입방(fcc) 구조의 δ-Bi2O3로 전환된다. δ-Bi2O3를 냉각시키면 650oC에서 정방정(tetragonal) 구조의 β-Bi2O3로 전환되거나 또는 639oC에서 체심입방(bcc) 구조의 γ-Bi2O3가 된다. β-Bi2O3는 303oC에서, 그리고 γ-Bi2O3는 500oC에서 α-Bi2O3로 전환된다. 녹는점은 824oC이다. Bi2O3는 염기와 반응하여 BiO2-와 BiO33-가 되는데, 이들은 고분자 음이온 형태로 중합된다. 예로, Li3BIO3와 Na3BiO3의 음이온은 실제로는 각각 Bi8O2424-와 Bi4O1212-이다. Bi2O3는 물에 녹지 않으며, 산에 녹아 Bi3+의 염을 생성한다. 다른 금속 산화물과 결합하여 혼합산화물을 만들고, 세라믹 제조 과정에 첨가하면 제조 온도를 낮추어 에너지 절감 효과를 가져온다. 안료로 연단(red lead, Pb3O4) 대신 사용되며, 불꽃 놀이에도 사용된다.
Bi2O4는 과산화비스무트로도 불리는데, 비스무트산 소듐(NaBiO3)을 질산으로 분해시키거나 뜨거운 묽은 알칼리 용액에 분산된 Bi2O3를 산화시키면 얻어진다. 갈색이고, 보통 1-2개의 물 분자로 수화되어 있으며, 무수물은 100oC까지는 안정하나, 보다 높은 온도에서는 분해한다. 물에 녹지 않으나 느리게 분해하며, 뜨거운 산에는 녹아 분해된다. 강한 산화제로, HCl를 Cl2로 산화시킨다. 금속 사출에서 윤활제로 사용된다. Bi2O5는 Bi2O3의 뜨거운 진한 알칼리 용액을 전기분해시키면 얻어지는데, 불안정하고 가열하면 산소를 발생시키고 분해된다.
칼코겐화물
비스무트는 칼로겐(Z, Z=S, Se, Te)과 Bi2Z3형의 칼코겐화물을 만드는데, 이들은 진성반도체(intrinsic semiconductor)로 띠 간격은 Bi2S3는 1.3eV, Bi2Se3는 0.35eV, Bi2Te3는 0.14eV이다. 이들은 500~900oC에서 해당 원소들 간의 반응으로 만들 수 있으나, Bi2S3는 보통 Bi3+ 염과 황화수소(H2S)를 반응시켜 얻는다. Bi2S3는 휘창연(bismuthinite)으로 자연 상태에도 존재한다. 녹는점이 775oC인 갈색 고체로, 물에 녹지 않으나 산에 녹아 H2S를 생성한다. 다른 비스무트 화합물을 만드는 출발 물질로 사용된다. Bi2Se3는 녹는점이 706oC인 진한 회색 물질로, 물에 녹지 않으나, 강한 산에 녹는다. 열전 성질이 있다. Bi2Te3는 녹는점이 585oC인 회색 물질로, 물에 녹지 않으나 느리게 분해한다. 실온에서 탁월한 열전 성질을 보이는 물질로, 전자공업에서 반도체 재료로 사용된다.
할로겐화물
비스무트의 삼할로겐화물(BiX3, X=F, Cl, Br, I) 4가지는 모두 시판되고 있어 구매가 가능하다. BiF3는 Bi2O3와 HF의 반응으로 쉽게 얻을 수 있으며, 녹는점이 649oC인 회백색 고체이다. 결정 구조가 서로 다른 α형과 β형의 두 가지가 있으며, 물에는 녹지 않으나, 진한 HF에 녹아 착화합물을 만든다. BiF5를 합성하는 원료물질로 사용된다. 다른 BiX3들도 Bi2O3와 HX의 반응으로 얻거나, Bi와 X2의 직접 반응으로 얻는다. BiCl3와 BiBr3는 물에서 쉽게 가수분해되어 BiOX(X = Cl, Br)가 되는데, BiOX은 물에서 BIO+와 X-로 해리된다. BiCl3는 녹는점이 227oC인 연한 노란색 흡습성 고체로, 메탄올, 아세톤, 에테르 등 유기용매에도 잘 녹으며, HCl과 반응하여 HBiCl4가 된다. 환원제에 의해 금속 비스무트로 쉽게 환원된다. 마이클(Michael) 반응, 무카이야마-알돌(Mukaiyama-aldol) 반응 등에 촉매로 사용되고, 다른 비스무트 염의 제조에도 사용된다. BiBr3는 녹는점이 218oC인 노란색 고체로, 물과 알코올에는 거의 녹지 않으나, 묽은 HCl과 KX (X=Cl, Br, I) 수용액에 녹는다. BiI3는 녹는점이 408.6oC인 검은색 고체로, 물에는 거의 녹지 않으나, KI, HI, HCl 수용액, 알코올에는 녹는다. 공기에 오래 노출되면 Bi(IO3)3로 변환된다.
비스무트의 오할로겐화물은 BiF5만 알려져 있는데, BiF3를 높은 온도에서 F2 또는 ClF3와 반응시켜 얻는다. 녹는점이 151.4oC인 무색의 바늘 모양 결정으로, 120oC에서 승화한다. 강한 플루오린화 시약이며, 산화력 또한 매우 크다. 물과 반응하여 오존(O3)과 이플오르화산소(OF2)를 생성하고 BiF3가 되며, 실온에서 아이오딘(I2)이나 황(S)과도 격렬하게 반응한다. 50oC 이상에서 파라핀오일(탄화수소)을 플루오르화탄소로, 150oC에서 UF4를 UF6로, 180oC에서 Br2를 BrF3로, 그리고 Cl2를 ClF로 변환시킨다. 또한 XeF4와 반응하여 [XeF3]+ 양이온을 만든다. 독성이 매우 크며, 점막, 피부, 눈, 호흡기에 자극을 준다.
BiF5 + XeF4 → [XeF3]+[BiF6]-
보다 낮은 산화 상태의 할로겐화물들도 알려져 있는데, 이들은 흔히 Bi3+, Bi53+, Bi82+, Bi95+와 같은 비스무트 뭉치 양이온을 포함하고 있다. BiCl이라고 여겨졌던 화합물은 Bi95+ 양이온과 BiCl52-, Bi2Cl82- 음이온의 복합체임이 밝혀졌다. 그러나 BiI는 사합체인 Bi4I4사슬로 이루어져 있으며, 가열하면 BiI3와 Bi로 분해된다. |






 수치로 보는 비스무트
수치로 보는 비스무트
 홀 계수(Hall coefficient)
홀 계수(Hall coefficient)