|
아스타틴 화합물

아스타틴은 반감기가 매우 짧은 방사성 원소이고 생산량도 극 미량이어서, 이 원소나 화합물이 무게를 잴 수 있을 정도의 양만큼 만들어지지 않지 않았으며, 따라서 특성들도 별로 알려지지 않았다. 아스타틴화수소(HAt)와 산소산 음이온(AtO-, AtO3-, AtO4-)에 대해서는 ‘화학적 성질’ 항에 소개되었으며, 여기서는 기타 아스타틴화물, 할로겐간 화합물, 그리고 유기화합물 유도체에 대해 소개한다.
아스타틴화물
원소 상태의 At 또는 AtI를 환원제(Zn/H+, SO2, SO3, SO3-/OH- 등)로 처리하면 아스타틴화 음이온(At-)이 되며, I- 이온 존재 하에서 At- 용액에 Ag+, Tl+, Pd2+, 또는 Pb2+ 등을 첨가하면 해당 금속의 아이오드화염과 아스타틴화염이 함께 침전된다.
할로겐간 화합물(Interhalogen compounds)
아스타틴은 기체 상태에서 다른 할로겐 원소(X2)와 반응하여 2원자 분자 상태의 할로겐간 화합물 AtX(X=Cl, Br, I)를 만든다. 또한, AtBr은 At와 IBr의 수용액과의 반응, 그리고 AtI는 At와 I2/I-용액과의 반응으로도 얻어진다. AtX는 CCl4나 이소프로필 에테르(i-Pr2O) 등의 유기용매로 추출될 수 있다. AtX는 과량의 할로겐이온이 있으면 삼할로겐 이온을 만드는데, 25oC에서 AtI + Cl-  AtICl-, AtI + Br- AtICl-, AtI + Br-  AtIBr-, AtI + I- AtIBr-, AtI + I-  AtI2-, AtBr + Br- AtI2-, AtBr + Br-  AtBr2- 반응들의 평형상수는 각각 9, 120, 2000, 320 M-1로 얻어졌다. 이들 삼할로겐 이온들은 CCl4로 추출되지 않는다. AtBr2- 반응들의 평형상수는 각각 9, 120, 2000, 320 M-1로 얻어졌다. 이들 삼할로겐 이온들은 CCl4로 추출되지 않는다.
아스타틴의 유기 화합물 유도체
아스타틴이 탄소에 직접 결합된 RAt, RAtCl2, R2AtCl, 그리고 RAtO2(R은 phenyl 또는 p-tosyl)들이 합성되었다. 아스타토벤젠(astatobenzene, PhAt)은 아이오도벤젠(iodobenene, PhI)을 AtI 또는 At-와 반응시켜 얻으며, PhN2Cl와 At-와의 반응에서도 생성된다. 한편, PhAt을 염소(Cl2)와 반응시키면 PhAtCl2가 생성되며, 이를 HgPh2와 반응시키면 Ph2AtCl이 얻어지고, NaOCl과 반응시키면 PhAtO2가 얻어진다. |
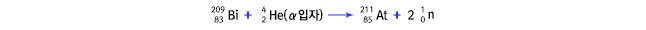



 수치로 보는 아스타틴
수치로 보는 아스타틴



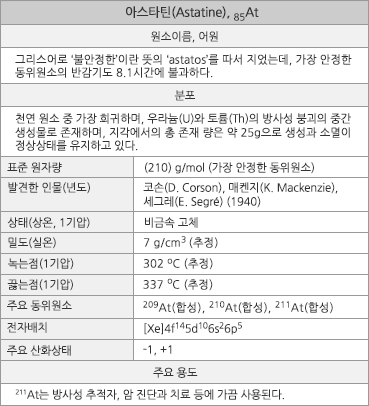


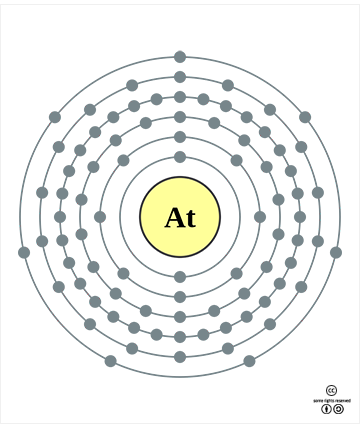
 AtICl-, AtI
AtICl-, AtI 