|
|
|
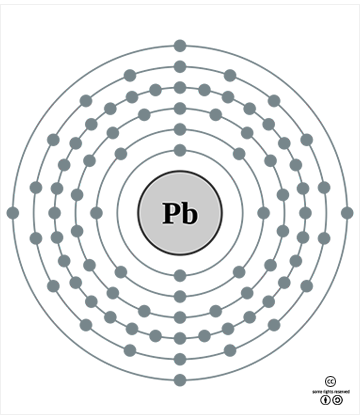
원자번호 82번 납 |
납의 원소정보 |
|
|
|
로마시대에 사용된 꼭지가 달린 납 수도관 <출처: © G.dallorto> |
로마시대 목욕탕의 납 배관 <출처: (cc) Zureks at Wikipedia.org> |
|

표면이 산화된 고순도 납 단괴에 둘러싸인 고순도 납 입방체 <출처: (cc) Alchemist-hp at Wikimedia.org>
|
|
|
|
|

방연석(Galena). 방연석은 가장 중요한 납 광석으로 화학적으로는 황화납(PbS)이다. <출처: (cc) Rob Lavinsky / iRocks.com>
|

납축전지. 납은 주로 자동차용 납축전지에 사용되는데, 납축전지는 이산화납(PbO2)을 양극, 납을 음극으로 하고 전해질로는 황산을 사용한다. <출처: gettyimage>
|
|
납 페인트. 납 화합물들이 여러 색상의 페인트 안료로 사용되었는데, 지금은 납의 환경오염 때문에 대부분 사용이 금지되었다. <출처: gettyimage> |
납 유리. PbO 함량이 보통 12~40%인 유리를 납 유리라 하는데, 굴절률이 높아 장식용으로 사용되고, 전자파 차단 유리로 전자제품에도 사용된다. 크리스탈 유리가 대표적인 납 유리이다. <출처: (cc) Canon50Dshooter at Wikimedia.org> |
|
|
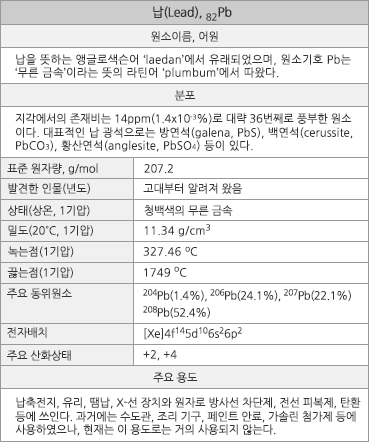
 수치로 보는 납
수치로 보는 납
납의 표준원자량은 207.2g/mol이고 원자의 바닥상태 전자배치는 1s22s22p63s23p63d104s24p64d105s25p64f145d106s26p2 ([Xe]4f145d106s26p2)이다. 지각에서의 존재비는 약 14ppm(1.4x10-3%)이며, 대략 36번째로 풍부한 원소이다. 녹는점은 327.46oC고 끓는점은 1749oC이며, 녹음열과 증발열은 각각 4.77kJ/mol과 179.5kJ/mol이다. 20oC에서 밀도는 11.34g/cm3이며, 모스 경도는 1.5이다. 화합물에서의 주된 산화수는 +2과 +4이다. 첫 번째, 두 번째, 세 번째 이온화 에너지는 각각 715.6, 1450.5, 3081.5 kJ/mol이며, 폴링의 전기음성도는 2.33이다. 20oC에서 전기비저항은 208 nΩ∙m 이고, 열전도율은 35.3 W∙m-1∙K-1이다. 원자반경은 175pm이고 6배위된 Pb2+의 이온반경은 119pm이다. 자연 상태의 동위원소는 204Pb(1.4%), 206Pb(24.1%), 207Pb(22.1%), 208Pb(52.4 %)의 4가지인데, 모두 안정한 것으로 볼 수 있다. 2012년의 전세계 신규 납 생산량은 520만 톤으로 추정된다.
발행일 2013.04.12
Lead
Lead pipes have been in use for thousands of years. In some cases the same pipe the whole time. This exotic six-way union was hand made by an apprentice decades ago, and it duly impressed the master. Scroll down to see examples of Lead. | |||||||||||||||||
'Natural science > 화 학' 카테고리의 다른 글
| Polonium(Po), 84-폴로늄 (0) | 2013.05.15 |
|---|---|
| Bismuth(Bi), 83-비스무트 (0) | 2013.05.15 |
| Thallium(Tl), 81-탈륨 (0) | 2013.05.15 |
| Mercury(Hg), 80(수은) (0) | 2013.05.15 |
| Gold(Au)- 79(금) (0) | 2013.05.15 |





 Pb2+ (1.1 M HClO4) Eo
Pb2+ (1.1 M HClO4) Eo